07/11/2023
Imagina poder encender una luz usando algo tan simple como un limón. Aunque parezca sacado de una película de ciencia ficción o un truco de magia, es un experimento real y fascinante que puedes hacer en casa con materiales comunes. Los limones, con su jugo ácido, pueden convertirse en una batería simple capaz de generar suficiente electricidad para encender un pequeño LED. Este proyecto no solo es divertido y visualmente interesante, sino que también es una excelente manera de aprender sobre los principios básicos de la electricidad, las reacciones químicas que generan energía y cómo funcionan las baterías.

La ciencia a menudo se esconde en los lugares más cotidianos, y este experimento con un simple cítrico es una prueba fascinante. Al comprender cómo funciona una batería de limón, desbloqueas la comprensión de conceptos como el voltaje, la corriente, los circuitos y la electroquímica, que son fundamentales en innumerables tecnologías que usamos a diario.

¿Qué es una Batería de Limón y Cómo Funciona?
Lo que creamos al usar limones, metales y cables es una batería voltaica casera, también conocida como celda electroquímica simple. No es una batería con la potencia de las que usas a diario en tus dispositivos electrónicos, pero sí genera una pequeña corriente eléctrica a través de una reacción química.
¿Cómo es posible que un limón genere electricidad? La clave está en la química que ocurre entre el jugo ácido del limón (el electrolito), que contiene iones (partículas cargadas eléctricamente), y dos metales diferentes (los electrodos), típicamente zinc y cobre. Cuando insertas un trozo de zinc (como el recubrimiento de un clavo galvanizado) y un trozo de cobre (como un cable de cobre puro o una moneda antigua de cobre) en el limón, estableces los dos terminales de una celda electroquímica con diferentes potenciales. Esto crea una diferencia de potencial, es decir, un voltaje.

El zinc es un metal más reactivo que el cobre en un ambiente ácido. En el clavo de zinc (que actúa como el ánodo, el terminal negativo de nuestra batería), los átomos de zinc reaccionan con el ácido del limón, perdiendo electrones y disolviéndose lentamente en el jugo como iones de zinc positivos (Zn²⁺). Estos electrones libres (e⁻) se acumulan en el clavo. En el trozo de cobre (que actúa como el cátodo, el terminal positivo), los iones de hidrógeno positivos (H⁺) presentes en el jugo ácido aceptan estos electrones libres que llegan a través de un circuito externo que conecta el ánodo y el cátodo, formando gas hidrógeno (H₂). El flujo de estos electrones a través del cable que conecta el zinc y el cobre externamente es lo que genera la corriente eléctrica que puede encender el LED. La diferencia de potencial, o voltaje, entre el ánodo y el cátodo es lo que 'empuja' estos electrones a través del circuito. Es, en esencia, una pequeña bomba que mueve cargas.
¿Cuántos Limones Necesitas para Encender un LED?
Una sola "batería" de limón (un limón con su clavo de zinc y su trozo de cobre) genera una pequeña diferencia de potencial. Típicamente, este voltaje está en el rango de 0.7 a 1 voltio. Sin embargo, un LED (Diodo Emisor de Luz) promedio requiere un voltaje mínimo para comenzar a brillar, generalmente entre 1.5 y 2 voltios, dependiendo del color y tipo específico del LED (los rojos suelen requerir menos voltaje que los verdes o azules).
Para alcanzar el voltaje necesario para encender el LED, no basta con un solo limón. Necesitarás conectar varias de estas celdas de limón en serie. Conectar baterías en serie significa unir el terminal negativo (el clavo de zinc) de una celda con el terminal positivo (el trozo de cobre) de la siguiente celda, y así sucesivamente. Al hacer esto, los voltajes de cada limón se suman. Si cada limón produce aproximadamente 0.7 a 1 voltio, conectar 3 limones en serie te daría entre 2.1 y 3 voltios, que suele ser suficiente para la mayoría de los LEDs. Conectar 4 limones te daría aún más voltaje (entre 2.8 y 4 voltios), lo que probablemente hará que el LED brille más intensamente. Generalmente, con 3 o 4 limones conectados correctamente en serie, tendrás suficiente voltaje para encender un LED rojo o amarillo. Tener 5 o 6 limones a mano puede ser útil para asegurar que alcanzas el voltaje necesario o para experimentar con un brillo mayor.
Es importante recordar que, aunque el voltaje es clave para 'empujar' la corriente, la cantidad de corriente (el flujo de electrones) que una batería de limón puede suministrar es muy baja. Esta baja corriente es la razón por la que solo puede alimentar dispositivos que consumen muy poca energía, como un LED, y no algo que requiera más potencia como una bombilla incandescente o un motor pequeño.
Materiales que Necesitarás
Para llevar a cabo este experimento científico y ver la luz del limón, reúne los siguientes elementos:
Limones: Se recomiendan al menos 4, pero tener 5 o 6 puede darte más margen para el éxito y la experimentación.
Clavos galvanizados: Necesitarás uno por cada limón que uses. Los clavos galvanizados están recubiertos de zinc, esencial para la reacción.
Trozo de cable de cobre o monedas de cobre antiguas: Necesitarás uno por cada limón. Busca cable de cobre puro (de una ferretería, por ejemplo) o monedas hechas predominantemente de cobre (verifica las fechas en tu país; en EE. UU., las monedas de un centavo anteriores a 1996 son buenas). La longitud del cable no es crítica, unos pocos centímetros por pieza son suficientes.
Cables con pinzas de cocodrilo: Necesitarás un número de cables igual al número de limones que uses, más uno adicional. Por ejemplo, si usas 4 limones, necesitarás 5 cables.
Un LED de bajo voltaje: Un LED rojo o amarillo suele ser una buena opción para empezar, ya que generalmente requieren menos voltaje para encenderse que los verdes o azules.
Opcional: Un voltímetro o multímetro para medir el voltaje que produces. Esto es muy útil para entender lo que está pasando y para solucionar problemas si el LED no se enciende.

Pasos para Construir tu Batería de Limón
Sigue estas instrucciones cuidadosamente para convertir tus limones en una fuente de energía:
1. Prepara los limones: Coloca cada limón sobre una superficie firme (como una mesa o encimera). Rueda cada limón vigorosamente sobre la superficie presionando con la palma de la mano. El objetivo es ablandar la pulpa interna del limón y romper las pequeñas bolsas de jugo para liberar tanto jugo como sea posible dentro de la cáscara. Esto asegura un mejor contacto entre los metales y el electrolito ácido. Ten cuidado de no romper la cáscara exterior del limón.
2. Inserta los electrodos: Haz dos pequeñas incisiones en la cáscara de cada limón, separadas entre sí unos centímetros. En una incisión, inserta un clavo galvanizado. En la otra incisión, inserta el trozo de cable de cobre o la moneda de cobre. Asegúrate de que ambos metales estén bien dentro de la pulpa jugosa del limón, pero es absolutamente crucial que *no se toquen* entre sí dentro del limón. Si se tocan, crearán un cortocircuito y no generarán voltaje útil.
3. Conecta las baterías en serie: Ahora vas a conectar tus limones para formar una cadena. Usa los cables con pinzas de cocodrilo. Conecta la pinza de un cable al clavo (el zinc) de un limón. Conecta la otra pinza del mismo cable al trozo de cobre (el cátodo) del *siguiente* limón en tu fila. Repite este proceso: conecta el clavo del segundo limón al cobre del tercer limón, el clavo del tercer limón al cobre del cuarto, y así sucesivamente. Deberás usar un cable menos que el número de limones para hacer estas conexiones 'en serie'.
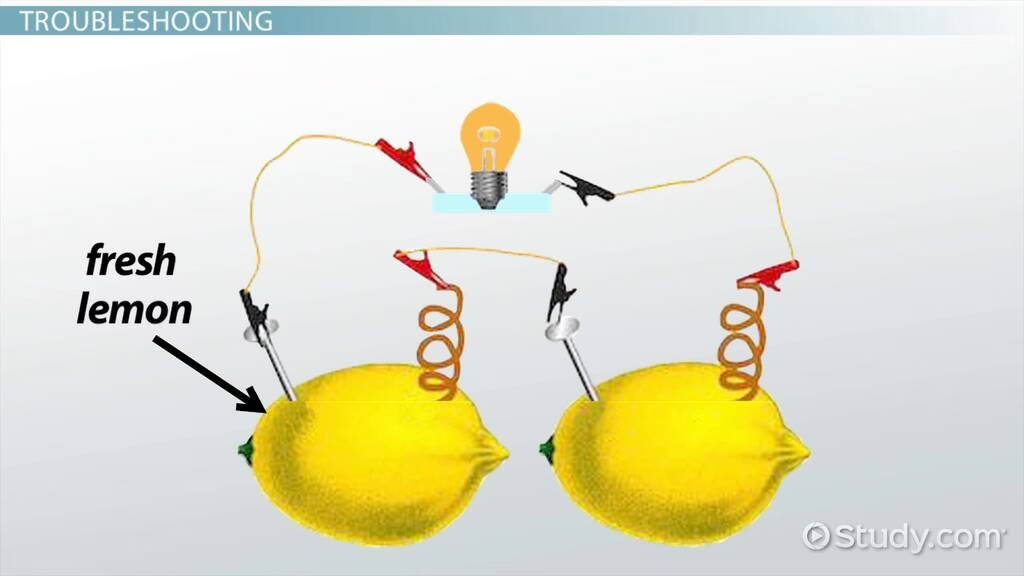
4. Conecta el LED: Al final de tu cadena de limones conectados en serie, tendrás un clavo libre en el primer limón y un trozo de cobre libre en el último limón. Estos son los terminales de tu batería de limón combinada. El clavo libre es el terminal negativo (ánodo del primer limón) y el cobre libre es el terminal positivo (cátodo del último limón). Conecta un cable con pinzas desde el clavo libre a una de las patas del LED. Conecta otro cable con pinzas desde el trozo de cobre libre a la otra pata del LED. ¡Presta mucha atención a la polaridad del LED! Los LEDs solo funcionan cuando la corriente fluye en la dirección correcta. Generalmente, la pata más larga del LED es el terminal positivo (ánodo del LED) y debe conectarse al terminal positivo de tu batería (el cobre al final de la cadena de limones). La pata más corta del LED es el terminal negativo (cátodo del LED) y debe conectarse al terminal negativo de tu batería (el clavo al principio de la cadena de limones). Si conectas el LED y no se enciende, simplemente invierte las conexiones en las patas del LED. Esta es la causa más común de que no funcione.
Consejos para Solucionar Problemas (Troubleshooting)
Si has seguido los pasos y tu LED no se enciende, no te desesperes. Aquí tienes algunas cosas que puedes revisar y probar:
- Verifica las conexiones: Asegúrate de que todas las pinzas de cocodrilo estén haciendo un contacto firme y seguro tanto con los metales insertados en los limones como con los extremos de los cables y las patas del LED.
- Espaciado de los metales: Revisa cuidadosamente que el clavo y el trozo de cobre no se estén tocando dentro de ningún limón. Si se tocan, no se generará voltaje útil.
- Polaridad del LED: Confirma que has probado ambas orientaciones del LED en los terminales de la batería de limón. Como mencionamos, los LEDs son polarizados y solo funcionan en una dirección.
- Preparación del limón: ¿Rodaste los limones con suficiente fuerza? Un limón bien ablandado libera más jugo, lo que mejora el contacto entre los metales y el electrolito ácido.
- Calidad de los materiales: Asegúrate de que estás usando clavos *galvanizados* (recubiertos de zinc) y trozos de cobre puro. Algunas monedas modernas son de zinc recubierto de cobre; si el recubrimiento está dañado, pueden no funcionar bien. Si sospechas que los metales están oxidados, puedes lijar ligeramente las superficies para exponer metal fresco.
- Añade más limones: Si estás usando solo 3 limones, intenta añadir un cuarto, un quinto o incluso un sexto limón a tu cadena en serie. Esto aumentará el voltaje total y puede ser justo lo que necesitas para alcanzar el umbral de tu LED.
- Usa un voltímetro (si tienes): Si tienes acceso a un voltímetro o multímetro, es una herramienta invaluable. Conéctalo a los terminales libres de tu cadena de limones (el clavo al principio y el cobre al final). Deberías medir un voltaje que aumenta con cada limón que añades (aproximadamente 0.7-1V por limón). Si el voltaje total es inferior a 1.5V (o el voltaje requerido por tu LED específico), sabes que necesitas más limones o mejorar la preparación. También puedes medir el voltaje de cada limón individualmente para identificar si alguno no está funcionando correctamente.
- Prueba otro LED: Es posible que el LED que estás usando esté defectuoso o que requiera un voltaje ligeramente mayor de lo que tu batería de limón puede proporcionar. Los LEDs de diferentes colores (verde, azul) suelen requerir un voltaje más alto que los rojos o amarillos.
- Prueba otro cítrico/patata: Si los limones no parecen funcionar bien, intenta con patatas o naranjas, que también contienen ácidos que actúan como electrolitos.
Explorando Más Allá: Variaciones y Extensiones
Una vez que logres encender el LED con limones, este experimento básico se puede expandir de varias maneras para seguir aprendiendo:
- Batería de patata: Las patatas también contienen ácido fosfórico y funcionan de manera muy similar a los limones como electrolitos. Prueba a construir una batería de patata siguiendo los mismos pasos.
- Otros cítricos o frutas: ¿Funcionan las naranjas, pomelos, limas o incluso manzanas? Experimenta con diferentes frutas y verduras ácidas para ver cuáles son los mejores electrolitos y si generan más o menos voltaje.
- Diferentes metales: Investiga y prueba otras combinaciones de metales (como hierro, aluminio, etc.) junto con el cobre o el zinc para ver cómo afectan el voltaje y la corriente generada. Necesitarás pares de metales con diferentes potenciales de oxidación.
- Alimentar otros dispositivos: Si consigues suficiente voltaje (quizás con más limones o patatas), podrías intentar alimentar otros dispositivos de muy bajo consumo que funcionen con una sola pila AA o AAA, como una pequeña calculadora LCD simple o un temporizador de cocina. Sin embargo, la corriente limitada seguirá siendo un desafío.

Preguntas Frecuentes
Aquí respondemos algunas dudas comunes sobre la batería de limón:
¿Por qué un limón y no otra fruta?
El limón es una opción popular y efectiva debido a su alto contenido de ácido cítrico, que sirve como un excelente electrolito que facilita el movimiento de iones necesario para la reacción electroquímica. Sin embargo, otras frutas y verduras ácidas, como las patatas (con ácido fosfórico), naranjas o pomelos, también pueden funcionar. La clave es la presencia de un ácido que pueda interactuar con los metales y actuar como electrolito.
¿Puedo encender una bombilla normal (incandescente) con limones?
No, definitivamente no. Las bombillas incandescentes requieren un voltaje (generalmente 1.5V, 3V, 6V, 12V, o más) y, lo que es más importante, una corriente eléctrica mucho mayor de la que una batería de limón puede proporcionar. Este experimento solo funciona con dispositivos de muy bajo consumo energético como los LEDs, que necesitan muy poca corriente para brillar.
¿Qué metales funcionan mejor?
La combinación más común y efectiva para este tipo de batería simple es zinc y cobre. Esto se debe a la diferencia en su reactividad química (potencial de oxidación), que impulsa el flujo de electrones. El zinc cede electrones fácilmente en un ambiente ácido, mientras que el cobre los acepta a través de los iones de hidrógeno. Otros pares de metales con potenciales electroquímicos diferentes también podrían funcionar, pero el zinc y el cobre son fáciles de conseguir (clavos galvanizados y cobre de cables o monedas antiguas) y proporcionan una diferencia de potencial útil.
¿Es peligroso este experimento?
En absoluto. La cantidad de electricidad generada por una batería de limón es extremadamente pequeña en términos de voltaje y corriente. No hay riesgo de descarga eléctrica ni de daño por calor con los materiales típicos usados en este experimento.
¿Qué sucede con el limón después del experimento?
El limón habrá participado en una reacción química. Los iones de zinc del clavo se habrán disuelto parcialmente en el jugo ácido, y se habrá producido una pequeña cantidad de gas hidrógeno (aunque a menudo no es visible). El limón no es apto para consumo después de usarlo como batería debido a la presencia de iones metálicos disueltos.
¿Es esta una fuente de energía práctica para la vida real?
No, de ninguna manera. La batería de limón es un excelente recurso educativo para demostrar principios electroquímicos y de circuitos básicos, pero no es una fuente de energía eficiente ni práctica para alimentar dispositivos en la vida real. La energía que produce es mínima, se agota relativamente rápido a medida que los metales se corroen y el ácido se neutraliza parcialmente, y es mucho más costosa y menos potente que las baterías comerciales.
¿Por qué algunos LEDs de colores funcionan mejor que otros?
Diferentes colores de LED (y diferentes tipos de LED del mismo color) tienen diferentes requisitos de voltaje para encenderse. Generalmente, los LEDs rojos y amarillos requieren menos voltaje (alrededor de 1.8-2.2V) que los verdes, azules o blancos (que pueden requerir 2.5-3.5V o más). Si tu batería de limón produce, por ejemplo, 2.5V, podría encender un LED rojo o amarillo brillantemente, un LED verde débilmente, y podría no encender un LED azul o blanco en absoluto. Experimentar con diferentes colores de LED es una buena forma de determinar el voltaje real que está produciendo tu batería de limón.
En resumen, encender un LED con limones es un proyecto educativo y entretenido que demuestra de forma tangible los principios básicos de cómo funcionan las baterías y cómo la química puede generar electricidad. Es una prueba de que la ciencia está presente en los lugares más inesperados, ¡incluso en tu frutero! Anímate a probarlo, sigue los pasos, soluciona los pequeños inconvenientes que puedan surgir y conviértete en un pequeño ingeniero eléctrico por un día mientras exploras el fascinante mundo de la electroquímica casera.
Si quieres conocer otros artículos parecidos a Ilumina un LED con Limones: El Experimento puedes visitar la categoría Maquillaje.
