22/08/2020
Un gas es uno de los cuatro estados fundamentales de la materia, junto con los sólidos, líquidos y plasmas. Lo que distingue a los gases es la gran separación entre sus partículas individuales (átomos o moléculas). Esta vasta separación es la razón por la que, a menudo, un gas incoloro resulta invisible para el observador humano.
Un gas puro puede estar compuesto por átomos individuales, como en el caso de los gases nobles (neón, argón), o por moléculas formadas por un solo tipo de átomo (elementos diatómicos como el oxígeno, nitrógeno) o por átomos diferentes (compuestos como el dióxido de carbono). Una mezcla de gases, como el aire que respiramos, contiene una variedad de gases puros.
El estado gaseoso se encuentra generalmente entre los estados líquido y plasma en la escala de temperatura. El plasma representa el límite superior de temperatura para los gases. En el extremo inferior de la escala de temperatura, encontramos gases cuánticos degenerados, que son objeto de creciente atención científica. Gases atómicos de alta densidad superenfriados a temperaturas muy bajas se clasifican como gases de Bose o gases de Fermi, basándose en su comportamiento estadístico.
Características Físicas de los Gases
Debido a que la mayoría de los gases son difíciles de observar directamente, se describen a través de cuatro propiedades físicas o características macroscópicas clave: presión, volumen, número de partículas (agrupadas en moles por los químicos) y temperatura. Estas características han sido estudiadas repetidamente por científicos pioneros, lo que llevó al desarrollo de relaciones matemáticas fundamentales, como la ley de los gases ideales.
Las partículas de gas están ampliamente separadas entre sí, y en consecuencia, tienen enlaces intermoleculares más débiles que los líquidos o los sólidos. Estas fuerzas intermoleculares, que surgen de interacciones electrostáticas, son responsables de muchas de las propiedades únicas de cada gas. Aunque las fuerzas intermoleculares en los gases son generalmente débiles, existen y varían entre sustancias, lo que influye en propiedades como los puntos de ebullición.
Comparados con otros estados de la materia, los gases tienen baja densidad y viscosidad. La presión y la temperatura influyen significativamente en las partículas dentro de un volumen dado. La variación en la separación y velocidad de las partículas se conoce como compresibilidad. Esta separación de partículas también afecta las propiedades ópticas de los gases, como se refleja en sus índices de refracción. Finalmente, las partículas de gas tienden a dispersarse o difundirse para distribuirse homogéneamente en cualquier recipiente.
Presión
La presión (o presión absoluta) de un gas en un recipiente se refiere a la fuerza promedio por unidad de área que el gas ejerce sobre las superficies del recipiente. Las partículas de gas se mueven en líneas rectas hasta que colisionan con las paredes del recipiente. La fuerza ejercida durante una colisión es el cambio en el momento de la partícula. La presión total es la suma de todas las componentes normales de fuerza ejercidas por las partículas que impactan las paredes, dividida por el área de la superficie.
Temperatura
La velocidad de una partícula de gas es proporcional a su temperatura absoluta. La temperatura de cualquier sistema físico está relacionada con el movimiento de las partículas que lo componen. En mecánica estadística, la temperatura es una medida de la energía cinética promedio almacenada en una molécula (también conocida como energía térmica). Esta energía se puede almacenar en diferentes modos (grados de libertad): traslación, rotación y vibración. Las moléculas de gas calentadas tienen un mayor rango de velocidades, con una velocidad promedio más alta. La distribución de velocidades se describe mediante la distribución de Maxwell-Boltzmann para gases ideales en equilibrio termodinámico.
Volumen Específico y Volumen
En análisis termodinámicos, se distingue entre propiedades intensivas y extensivas. Las propiedades que dependen de la cantidad de gas (masa o volumen) son extensivas (como el volumen V), mientras que las que no dependen de la cantidad son intensivas (como el volumen específico v). El volumen específico es la relación entre el volumen ocupado por una unidad de masa de un gas en equilibrio. Mil átomos de un gas ocupan el mismo espacio que otros mil átomos del mismo gas bajo las mismas condiciones de temperatura y presión.
Densidad
La densidad (ρ) es la cantidad de masa por unidad de volumen de una sustancia, o la inversa del volumen específico. Para los gases, la densidad puede variar considerablemente porque las partículas pueden acercarse o alejarse libremente, influenciadas por la presión o el volumen. Esta variación de densidad es la compresibilidad. La densidad es una variable de estado del gas, y su cambio durante un proceso termodinámico sigue las leyes correspondientes. Para un gas estático, la densidad es uniforme en todo el recipiente.
Visión Microscópica de los Gases
Si pudiéramos observar un gas con un microscopio muy potente, veríamos una colección de partículas sin forma o volumen definidos, en movimiento más o menos aleatorio. Estas partículas cambian de dirección solo al colisionar con otras partículas o con las paredes del recipiente. Esta visión microscópica se describe bien mediante la mecánica estadística y la teoría cinética de los gases.
Teoría Cinética de los Gases
La teoría cinética de los gases proporciona una comprensión de las propiedades macroscópicas (presión, temperatura) a partir del comportamiento microscópico de las partículas. Asumiendo colisiones perfectamente elásticas, relaciona la energía cinética promedio por molécula con la temperatura y la presión del sistema. Explica cómo el sistema responde a cambios de temperatura: al aumentar la energía, las partículas se mueven más rápido, colisionan con mayor frecuencia y fuerza contra las paredes, aumentando la presión y la temperatura macroscópica.
Movimiento Térmico y Mecánica Estadística
En gases reales, el movimiento térmico incluye traslación, rotación y vibración, no solo traslación lineal como en el modelo ideal. Los fenómenos cuánticos también influyen. El conjunto de posibles movimientos y partículas define los microestados del sistema. La mecánica estadística, utilizando la función de partición, conecta estos microestados con las variables macroscópicas medibles (temperatura, presión, energía interna, etc.). El teorema de equipartición puede simplificar cálculos, pero asume que todos los grados de libertad están igualmente poblados, lo cual no es siempre cierto (la capacidad calorífica varía con la temperatura).
Movimiento Browniano
El movimiento browniano describe el movimiento aleatorio de partículas suspendidas en un fluido (líquido o gas). Aunque las partículas de gas individuales tienen un movimiento aleatorio, el movimiento browniano observado de partículas más grandes suspendidas es el resultado de colisiones desiguales con muchas moléculas de gas, creando un movimiento errático pero menos abrupto que el de una sola molécula de gas.
Gases Ideales vs. Gases Reales
La diferencia principal entre gases ideales y reales radica en las fuerzas intermoleculares.
Fuerzas Intermoleculares
Las fuerzas entre dos o más moléculas, atractivas o repulsivas, son fundamentales para modelar sistemas moleculares y predecir propiedades físicas. Las fuerzas de Van der Waals son un ejemplo prominente, cruciales para propiedades como la viscosidad. Ignorar estas fuerzas (dependientes de la proximidad) permite tratar un gas real como ideal, simplificando los cálculos.
La interacción entre dos moléculas se modela a menudo con el potencial de Lennard-Jones, que combina una atracción de largo alcance (fuerza de dispersión de London) y una repulsión de corto alcance (interacción de intercambio electrónico). La atracción es significativa a bajas velocidades (baja temperatura) y bajas presiones. La repulsión domina a altas velocidades (alta temperatura) y altas presiones, o cuando las moléculas están muy cerca.
Considerando estos efectos, los gases reales se desvían del modelo ideal:
- A bajas temperaturas y bajas presiones, el volumen ocupado por un gas real es menor que el predicho por la ley de los gases ideales (predominan las atracciones).
- A altas temperaturas y altas presiones, el volumen ocupado por un gas real es mayor que el predicho (predominan las repulsiones al estar muy cerca, o el tamaño propio de las moléculas se vuelve relevante).
Modelos Matemáticos y Leyes de los Gases
Una ecuación de estado describe o predice las propiedades de un gas. No existe una única ecuación para todos los gases en todas las condiciones, por lo que se han desarrollado varios modelos.
Gas Ideal y Gas Perfecto
La ecuación de estado más conocida es la ley de los gases ideales:
PV = nRT
Donde P es presión, V es volumen, n es cantidad de gas (moles), R es la constante universal de los gases y T es temperatura. También puede escribirse como P = ρRsT, donde ρ es densidad y Rs es la constante específica del gas.
Un gas ideal es un gas real simplificado con un factor de compresibilidad Z igual a 1. La ley de los gases ideales es adecuada para muchas aplicaciones de ingeniería, especialmente a presiones relativamente bajas y temperaturas moderadas.
El término "gas perfecto" a veces se usa para un gas ideal con la suposición adicional de que su capacidad calorífica es constante.
Gas Real
Los efectos de gas real incluyen correcciones para abarcar un rango más amplio de comportamiento, especialmente en condiciones extremas (altas presiones, altas temperaturas):
- Efectos de compresibilidad (Z ≠ 1)
- Capacidad calorífica variable (depende de la temperatura)
- Fuerzas de Van der Waals (consideradas en ecuaciones de estado más complejas)
- Efectos termodinámicos de no equilibrio
- Disociación molecular y reacciones químicas.
Estos efectos son significativos en situaciones como la reentrada atmosférica de vehículos espaciales o eventos geológicos de alta energía.
Gas Permanente
Un gas permanente es aquel cuya temperatura crítica está por debajo del rango de temperaturas habitables normales, lo que significa que no puede ser licuado solo por presión a temperatura ambiente. Históricamente, se pensaba que no se podían licuar, de ahí el término "permanente" en estado gaseoso. Esto es relevante para el almacenamiento y transporte de gases a alta presión.
Leyes Históricas de los Gases
El estudio de los gases condujo a varias leyes fundamentales:
| Ley | Científico | Año | Descripción | Relación (a T y n constantes) | Relación (a P y n constantes) | Relación (a V y n constantes) | Relación (a T y P constantes) |
|---|---|---|---|---|---|---|---|
| Boyle | Robert Boyle | 1662 | A T y n constantes, la presión es inversamente proporcional al volumen. | P ∝ 1/V (PV = k) | |||
| Charles | Jacques Charles | 1787 | A P y n constantes, el volumen es directamente proporcional a la temperatura absoluta. | V ∝ T (V/T = k) | |||
| Gay-Lussac | Joseph Louis Gay-Lussac | 1802/1809 | A V y n constantes, la presión es directamente proporcional a la temperatura absoluta. | P ∝ T (P/T = k) | |||
| Avogadro | Amedeo Avogadro | 1811 | A T y P constantes, volúmenes iguales de gases puros contienen el mismo número de partículas. El volumen es proporcional a la cantidad de sustancia (moles). | V ∝ n (V/n = k) | |||
| Dalton (Presiones Parciales) | John Dalton | 1801 | La presión total de una mezcla de gases no reactivos es la suma de las presiones parciales de cada gas. |
La ley de Dalton se expresa matemáticamente como: Ptotal = P1 + P2 + ... + Pn.
Conceptos Adicionales
Compresibilidad
El factor de compresibilidad (Z) es utilizado por los termodinamicistas para modificar la ecuación del gas ideal y tener en cuenta los efectos de compresibilidad de los gases reales. Representa la relación entre el volumen específico real y el ideal. Un valor Z cercano a la unidad indica comportamiento casi ideal. Se desvía de 1 a altas presiones y bajas temperaturas.
Capa Límite
Cuando un objeto se mueve a través de un gas, las partículas de gas tienden a "pegarse" a la superficie del objeto, formando una capa límite. Esta capa es prácticamente estática en la superficie debido a la fricción y efectivamente cambia la forma del objeto percibida por el resto del gas en movimiento. La separación de la capa límite puede alterar drásticamente el flujo del gas.
Turbulencia
En dinámica de fluidos, la turbulencia es un régimen de flujo caracterizado por cambios caóticos y estocásticos en las propiedades del fluido, como la velocidad y la presión. Implica baja difusión de momento, alta convección de momento y rápidas variaciones espaciales y temporales. Es un fenómeno complejo de modelar.
Viscosidad
La viscosidad es una medida de la resistencia interna de un fluido al flujo. Aunque los gases tienen menor viscosidad que los líquidos, no es nula. La viscosidad es lo que permite la formación de la capa límite en la superficie de los objetos.
Número de Reynolds
En mecánica de fluidos, el número de Reynolds es una relación adimensional entre las fuerzas de inercia y las fuerzas viscosas. Es crucial para determinar la similitud dinámica entre modelos a escala y situaciones reales, y para caracterizar el régimen de flujo (laminar o turbulento).
Principio de Máxima Entropía y Equilibrio Termodinámico
El principio de máxima entropía postula que un sistema evolucionará hacia el macroestado que corresponde a la mayor multiplicidad (mayor número de microestados posibles). El equilibrio termodinámico se alcanza cuando cesa la transferencia de energía dentro de un sistema y entre el sistema y su entorno. Esto implica que la temperatura, las fuerzas externas y las reacciones químicas están equilibradas.
Preguntas Frecuentes
¿Cuáles son los cuatro estados fundamentales de la materia? Los cuatro estados fundamentales de la materia son sólido, líquido, gas y plasma.
¿Qué diferencia principal hay entre un gas y un líquido o sólido? La principal diferencia es la gran separación entre las partículas individuales del gas, resultando en fuerzas intermoleculares mucho más débiles y ausencia de forma o volumen definidos.
¿Qué propiedades macroscópicas describen un gas? Las propiedades clave son presión, volumen, número de partículas (o moles) y temperatura.
¿Qué es un gas ideal? Un gas ideal es un modelo teórico que asume que las partículas de gas no tienen volumen propio y no interactúan entre sí (no hay fuerzas intermoleculares). Sigue la ley de los gases ideales (PV = nRT).
¿Cómo se diferencia un gas real de un gas ideal? Un gas real considera el volumen finito de las partículas y las fuerzas intermoleculares (atracciones y repulsiones), lo que causa desviaciones del comportamiento ideal, especialmente a altas presiones y bajas temperaturas.
¿Qué es la compresibilidad de un gas? Es la capacidad de un gas para disminuir su volumen bajo presión, debido a la gran separación entre sus partículas.
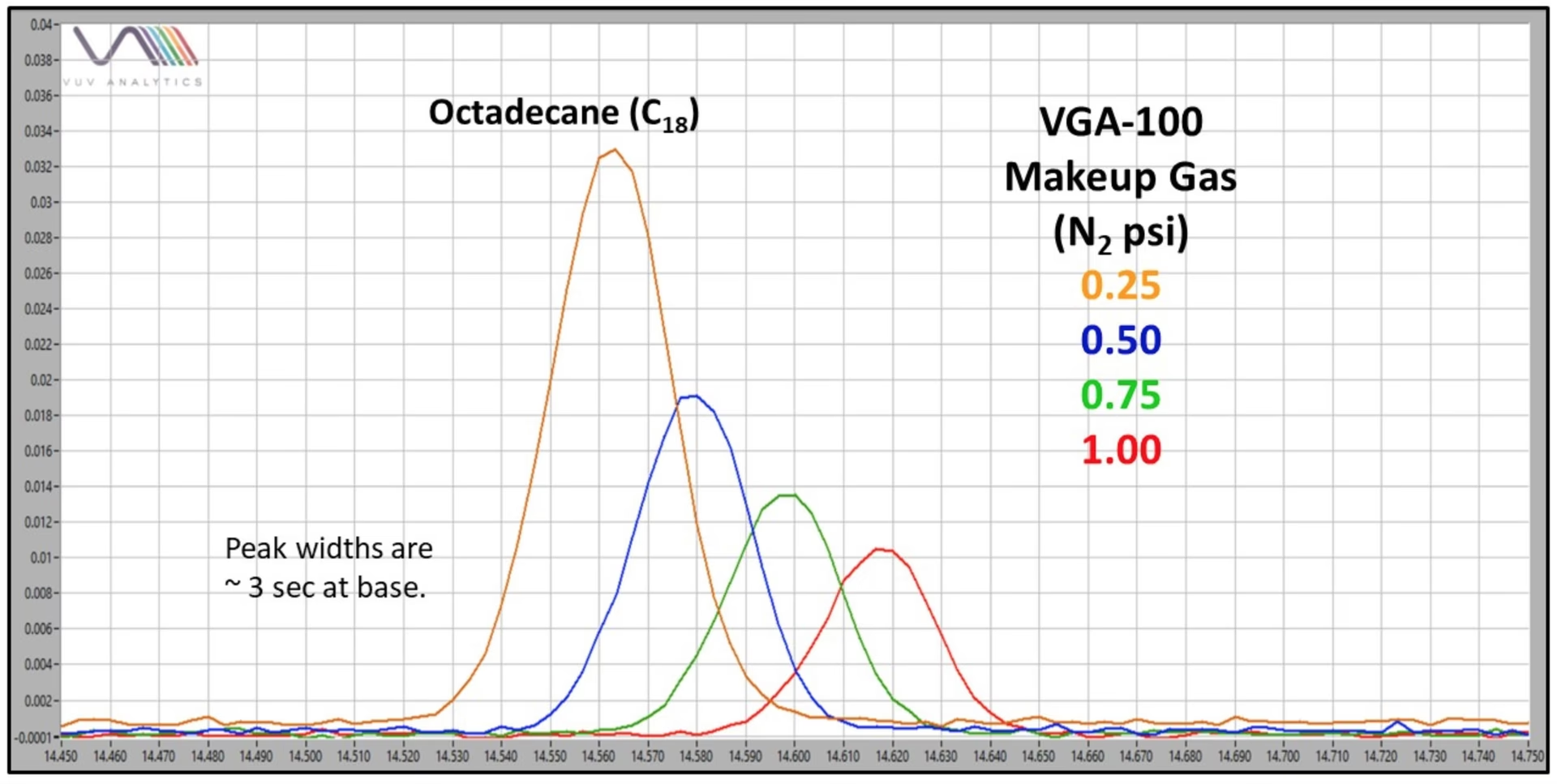
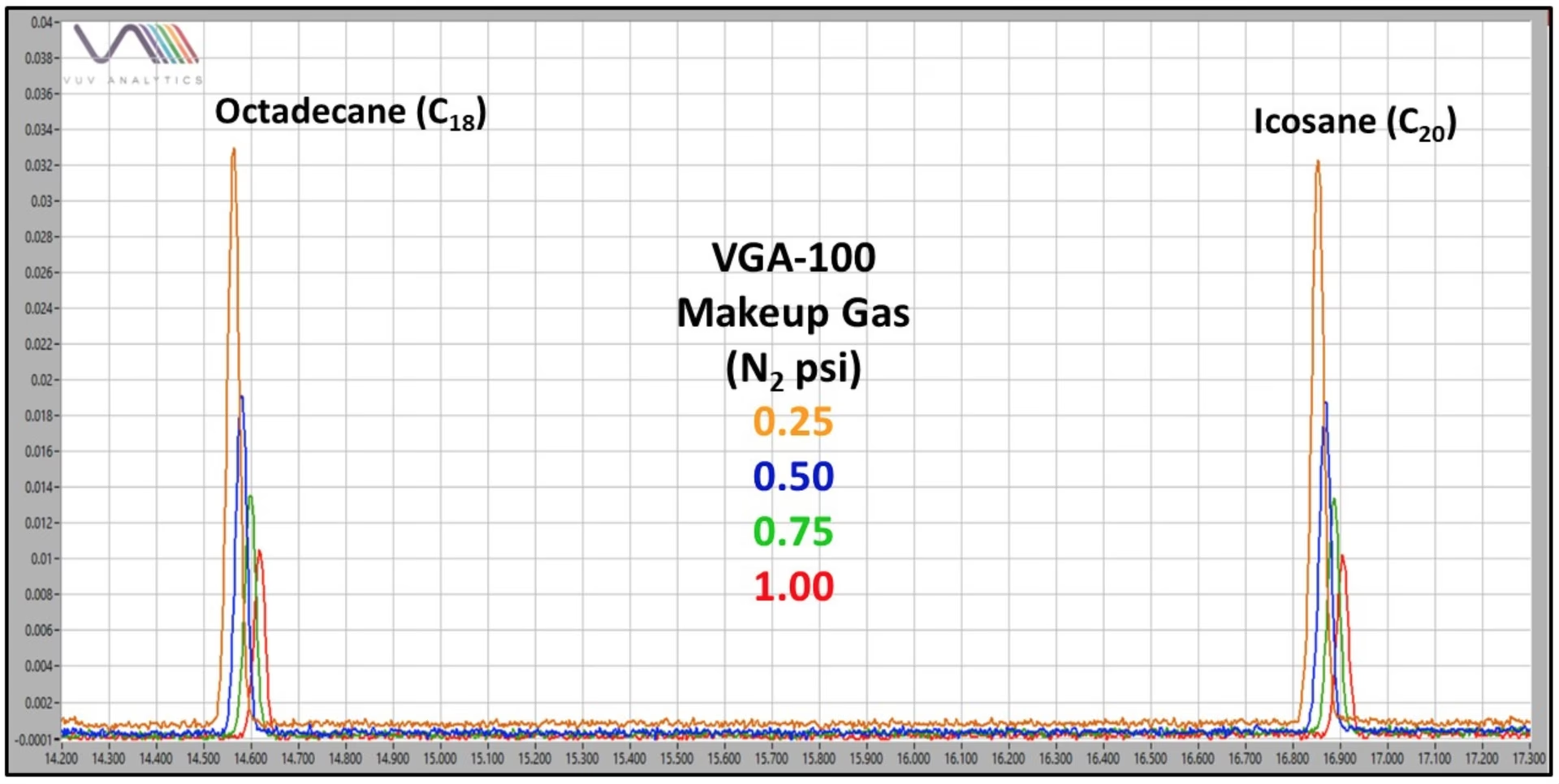
¿Qué es el "makeup gas" en cromatografía de gases? Es un gas auxiliar utilizado en ciertos detectores de cromatografía de gases para arrastrar eficientemente los analitos desde la columna a través del detector. Su flujo puede afectar la sensibilidad.
Si quieres conocer otros artículos parecidos a ¿Qué es un Gas? Naturaleza y Propiedades puedes visitar la categoría Maquillaje.