14/08/2022
El grafito es mucho más que la mina de tu lápiz. Es una forma cristalina del elemento carbono, conocida formalmente como un alótropo. A diferencia de su famoso pariente, el diamante, el grafito es oscuro, opaco, extremadamente blando y tiene un tacto grasiento que le permite dejar una marca negra, de ahí su nombre derivado del verbo griego graphein, que significa "escribir". Esta característica tan distintiva es solo la punta del iceberg de las propiedades y aplicaciones de este mineral extraordinario.

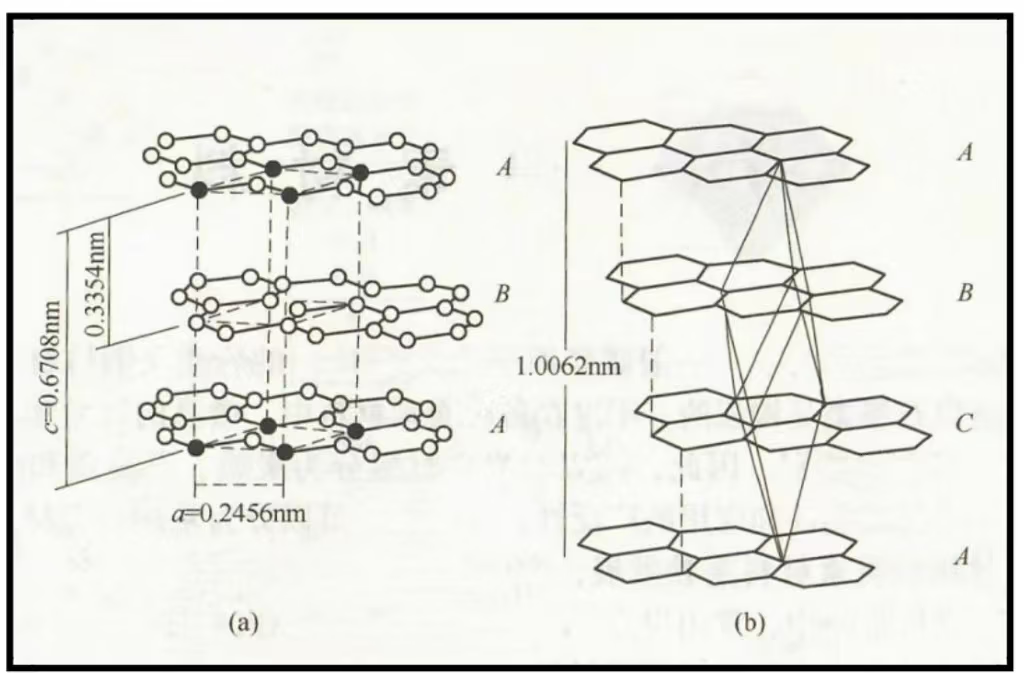
La singularidad del grafito reside profundamente en su estructura atómica. Consiste en láminas apiladas de grafeno, donde cada lámina es una red hexagonal de átomos de carbono unidos fuertemente. Estas láminas están dispuestas horizontalmente y separadas por una distancia relativamente grande. La unión dentro de las láminas es fuerte (enlaces covalentes sp2), pero la conexión entre las láminas es débil (fuerzas de van der Waals). Esta debilidad entre las capas permite que se deslicen fácilmente unas sobre otras, una característica que explica muchas de sus propiedades, como su suavidad y su capacidad lubricante.
Composición y Estructura Única
Químicamente, el grafito es simplemente carbono. Su fórmula química es C. Sin embargo, la forma en que los átomos de carbono se organizan es lo que le confiere sus propiedades únicas y lo diferencia de otros alótropos del carbono, como el diamante. Mientras que en el diamante los átomos de carbono están dispuestos en una estructura tridimensional rígida y tetraédrica, en el grafito forman estas distintivas capas bidimensionales.
El grafito natural puede presentarse en dos formas alotrópicas principales que difieren en el apilamiento de las capas de grafeno: la forma alfa (hexagonal), que es la más común y estable, y la forma beta (romboédrica), que es menos estable energéticamente y no se encuentra pura en la naturaleza, sino que suele constituir entre el 5% y el 15% del grafito natural o comercial. La forma beta puede convertirse en alfa mediante fuerzas de cizallamiento, y la alfa revierte a beta cuando se calienta a 1300 °C durante cuatro horas.
Esta estructura en capas no solo explica su blandura y lubricidad, sino también su conductividad eléctrica y térmica, aunque de manera anisótropa. La conductividad es mucho mayor paralela a las capas (donde los electrones deslocalizados pueden moverse libremente) que perpendicular a ellas.
Propiedades Físicas y Químicas Clave
Las propiedades del grafito lo hacen invaluable en una amplia gama de aplicaciones:
- Color y Textura: Es de color gris oscuro a negro, opaco, y tiene un tacto grasiento.
- Blandura: Con una dureza Mohs de 1-2, es uno de los minerales más blandos.
- Densidad: Su gravedad específica es de 1.9-2.3.
- Punto de Fusión: En ausencia de oxígeno, su punto de fusión supera los 3000 °C, siendo uno de los minerales más resistentes a altas temperaturas.
- Conductividad Eléctrica: Es un buen conductor de la electricidad debido a los electrones deslocalizados en las capas de carbono.
- Conductividad Térmica: También es un buen conductor del calor, especialmente paralelo a las capas.
- Lubricidad: Las capas que se deslizan fácilmente lo convierten en un excelente lubricante seco.
- Inercia Química: Es resistente a la mayoría de los productos químicos, aunque se oxida fácilmente en atmósferas con oxígeno a partir de unos 700 °C.
Es interesante notar la marcada diferencia entre el grafito y el diamante, ambos compuestos únicamente por carbono. Mientras el grafito es blando, conductor y oscuro, el diamante es el mineral más duro conocido, aislante eléctrico y generalmente transparente. Esta diferencia radical subraya cómo la estructura cristalina influye drásticamente en las propiedades de un material.
Grafito Natural vs. Sintético
El grafito se obtiene tanto de depósitos geológicos naturales como mediante procesos de fabricación humana. Existen diferencias clave entre ambos:
| Característica | Grafito Natural | Grafito Sintético |
|---|---|---|
| Origen | Depósitos geológicos (metamorfismo de rocas carbonáceas) | Producido artificialmente (calentamiento de materiales hidrocarbonados) |
| Pureza Típica | Varía según el depósito y procesamiento | Extremadamente alta (generalmente > 99.9% C) |
| Estructura | Puede contener formas amorfas, escamas o grumos; mezcla de alfa y beta | Altamente puro, generalmente forma alfa; puede formar escamas grandes |
| Densidad | Generalmente más alta | Generalmente más baja |
| Conductividad | Generalmente más alta | Generalmente más baja |
| Porosidad | Generalmente más baja | Generalmente más alta |
| Proceso de Producción | Minería, beneficio (flotación, lixiviación ácida) | Proceso Acheson (calentamiento a > 2100°C), CVD, etc. |
El grafito natural se extrae de minas a cielo abierto o subterráneas. Su procesamiento implica la separación del grafito de la ganga (roca estéril), a menudo mediante flotación por espuma, aunque esto puede ser desafiante debido a que el grafito blando recubre las partículas de ganga. Se requieren procesos repetidos de molienda y flotación o lixiviación ácida para obtener concentrados de alta pureza.
El grafito sintético se produce típicamente a partir de materiales hidrocarbonados, como el coque de petróleo, calentándolos a temperaturas superiores a 2100 °C, comúnmente utilizando el proceso Acheson. Estas altas temperaturas no solo forman el grafito sino que también volatilizan las impurezas, dando como resultado un producto de muy alta pureza. Aunque generalmente tiene menor densidad y conductividad que su equivalente natural, el grafito sintético puede formarse en escamas muy grandes y mantener una pureza excepcional, lo que lo hace ideal para ciertas aplicaciones de alta tecnología.
Aplicaciones Industriales y Tecnológicas
La versatilidad del grafito se refleja en su amplia gama de usos industriales:
Refractarios
El grafito es un material clave en la industria de los refractarios (materiales resistentes al calor). Se utiliza en crisoles para fundir metales, ladrillos de carbono-magnesita y formas de alúmina-grafito para revestir hornos de acero y canales de colada continua. Su alta estabilidad térmica y conductividad lo hacen ideal para soportar temperaturas extremas en procesos metalúrgicos.
Baterías
El grafito es el material de ánodo predominante en las baterías de iones de litio, que alimentan desde dispositivos electrónicos portátiles hasta vehículos eléctricos. Tanto el grafito natural como el sintético se utilizan en esta aplicación. La capacidad del grafito para intercalar iones de litio entre sus capas sin sufrir daños significativos por hinchazón es fundamental para el funcionamiento de estas baterías. La creciente demanda de vehículos eléctricos está impulsando significativamente el consumo de grafito de alta calidad.
Fabricación de Acero
En la fabricación de acero, el grafito natural se utiliza principalmente para aumentar el contenido de carbono en el acero fundido. También puede servir como lubricante para los troqueles utilizados en la extrusión de acero caliente. Aditivos de carbono como grafito sintético en polvo y coque de petróleo compiten en este mercado.
Revestimientos de Frenos
El grafito amorfo y de escama fina se utiliza en revestimientos de frenos, especialmente para vehículos pesados, como sustituto del amianto. Su capacidad lubricante ayuda a reducir el desgaste y el ruido.
Revestimientos de Fundición y Lubricantes
Se utiliza una suspensión acuosa de grafito (revestimiento de fundición) para cubrir el interior de los moldes, facilitando la separación del objeto fundido una vez enfriado. Los lubricantes de grafito son especiales, utilizados en condiciones de muy alta o baja temperatura, como lubricantes para troqueles de forja, agentes antiadherentes o lubricantes para cerraduras y maquinaria minera. El grafito coloidal (suspendido en un líquido) es una forma común de lubricante de grafito.
Electrodos
Los electrodos de grafito, especialmente los sintéticos, son cruciales en hornos de arco eléctrico para fundir chatarra de hierro y acero. Conducen la electricidad necesaria para generar el arco. También se utilizan en la electroerosión (EDM) para fabricar moldes.
Moderador de Neutrones
Grados especiales de grafito sintético se utilizan como matriz y moderador de neutrones en reactores nucleares. Su baja sección transversal de captura de neutrones lo hace adecuado, aunque es crucial que esté libre de impurezas como el boro.
Grafito Expandido y Compuestos
El grafito expandido, producido al intercalar ácidos entre sus capas, se utiliza para hacer láminas de grafito, juntas de alto rendimiento, cortafuegos y disipadores de calor para dispositivos electrónicos. Las fibras de grafito (fibra de carbono) se utilizan en materiales compuestos de alto rendimiento, como plásticos reforzados con fibra de carbono, empleados en aeroespacial, automoción y artículos deportivos. Estos compuestos aprovechan la alta resistencia y ligereza de las fibras de carbono.
Usos Cotidianos e Históricos
El uso más conocido del grafito es, sin duda, en los lápices. La capacidad de dejar una marca negra en el papel le dio su nombre y ha sido fundamental para la escritura y el dibujo durante siglos. La mina de lápiz moderna es una mezcla de grafito en polvo y arcilla, cuya proporción determina la dureza o blandura de la mina.
Históricamente, el grafito se conocía como plumbago o plomo negro, debido a su apariencia similar a los minerales de plomo, aunque químicamente no tienen relación. Grandes depósitos, como el de Borrowdale en Inglaterra (descubierto antes de 1565), fueron cruciales inicialmente para marcar ovejas y luego para usos militares (moldes para balas de cañón) debido a su pureza. En el siglo XIX, sus usos se expandieron enormemente a pulimentos, lubricantes, pinturas, crisoles y lápices.
Seguridad Ocupacional y Riesgos
Aunque el grafito en su estado manufacturado generalmente no presenta riesgos de inhalación, el polvo y los humos generados durante el procesamiento pueden ser peligrosos. La inhalación frecuente y prolongada de polvo de grafito puede irritar el sistema respiratorio y aumentar el riesgo de desarrollar neumoconiosis, una enfermedad pulmonar. Altas concentraciones de polvo también pueden irritar los ojos y la piel. Como cualquier polvo fino combustible, los altos niveles de polvo de grafito en el aire pueden crear un potencial de explosión.
En Estados Unidos, la OSHA ha establecido límites de exposición permisibles para el polvo de grafito en el lugar de trabajo (15 millones de partículas por pie cúbico o 1.5 mg/m3 como promedio ponderado en el tiempo de 8 horas para polvo total; NIOSH recomienda 2.5 mg/m3 para polvo respirable). A niveles muy altos (1250 mg/m3), el grafito se considera inmediatamente peligroso para la vida y la salud.
El Ciclo de Vida del Grafito: Minería y Reciclaje
La minería de grafito natural, aunque esencial para el suministro global, puede tener impactos ambientales negativos. Los principales países productores de grafito natural incluyen China, India, Brasil, Turquía y Corea del Norte.

El reciclaje de grafito es una práctica importante, especialmente para el grafito sintético utilizado en electrodos. Los restos de electrodos se trituran y clasifican, y el polvo resultante se utiliza a menudo para aumentar el contenido de carbono en el acero. Los refractarios que contienen grafito a veces se reciclan, aunque su bajo contenido de grafito puede dificultar la rentabilidad del proceso. Una fuente interesante de grafito reciclado es el kish de la fabricación de acero, un residuo rico en grafito que se puede procesar para obtener un producto de grafito de alta calidad.
Innovación y Futuro del Grafito
La investigación y el desarrollo en torno al grafito están en constante evolución, impulsados por la demanda de nuevas tecnologías, especialmente en el sector de las baterías. China lidera la innovación global en patentes relacionadas con el grafito, aunque otros países como Japón, Corea del Sur, Estados Unidos y Rusia también son importantes. El interés se centra tanto en mejorar los métodos de procesamiento del grafito natural (como la exfoliación) como en desarrollar nuevas formas y usos para el grafito sintético.
Las aplicaciones emergentes del grafito incluyen su uso en biomedicina, sensores y tintas conductoras, a menudo aprovechando las propiedades únicas de los nanomateriales de grafito, como el grafeno (una sola capa de átomos de carbono). Estos campos emergentes sugieren un futuro brillante y diverso para este fundamental mineral de carbono.
Preguntas Frecuentes sobre el Grafito
Aquí respondemos algunas preguntas comunes sobre este fascinante material:
P: ¿Es el grafito lo mismo que el plomo de los lápices?
R: No, no es lo mismo. Históricamente se le llamaba "plomo negro" o "plumbago" por su apariencia similar a los minerales de plomo, pero químicamente el grafito es carbono puro, mientras que el plomo es un metal diferente. Las minas de lápiz modernas son una mezcla de grafito y arcilla.
P: ¿Cuál es la fórmula química del grafito?
R: La fórmula química del grafito es simplemente C, ya que está compuesto exclusivamente por átomos de carbono.
P: ¿Por qué el grafito conduce la electricidad si el diamante, que también es carbono, no lo hace?
R: La diferencia está en su estructura atómica. En el grafito, los átomos de carbono forman capas hexagonales donde cada átomo está unido a otros tres. El cuarto electrón de valencia de cada átomo está deslocalizado y libre para moverse a lo largo de las capas, permitiendo la conducción eléctrica. En el diamante, todos los electrones de valencia están fuertemente unidos en una estructura tridimensional rígida, sin electrones libres para conducir.
P: ¿El grafito es peligroso?
R: En su forma sólida y manufacturada, generalmente no es peligroso. Sin embargo, la inhalación prolongada de polvo fino de grafito en el lugar de trabajo puede causar problemas respiratorios como la neumoconiosis. También existe un riesgo de explosión si se acumulan altos niveles de polvo fino en el aire.
P: ¿Para qué se usa el grafito además de los lápices?
R: Tiene numerosos usos industriales y tecnológicos, incluyendo refractarios (materiales resistentes al calor), ánodos en baterías (especialmente de iones de litio), aditivo de carbono en la fabricación de acero, revestimientos de frenos, lubricantes, electrodos, moderadores de neutrones en reactores nucleares, y como componente en compuestos de fibra de carbono.
En resumen, el grafito es un material de carbono con una estructura de capas única que le otorga una combinación de propiedades excepcional. Desde su humilde origen en los lápices hasta su papel crucial en tecnologías avanzadas como las baterías y los materiales compuestos, el grafito sigue siendo un pilar de la industria moderna y un foco de continua innovación. Su historia y sus aplicaciones demuestran el poder de la estructura atómica para definir la utilidad de un simple elemento.
Si quieres conocer otros artículos parecidos a Grafito: El Mineral Versátil del Carbono puedes visitar la categoría Maquillaje.
