17/10/2021
Hola, amantes del brillo y la belleza! Hoy vamos a tomar un pequeño desvío de nuestro universo de paletas y brochas para explorar algo un poco diferente, pero igual de fascinante: un proceso invisible que ocurre constantemente a nuestro alrededor, llamado ionización. Aunque no lo apliquemos directamente con una esponja, entender cómo funcionan las partículas a un nivel fundamental es sorprendentemente interesante. ¡Acompáñenme en este viaje científico!

En su esencia más pura, la ionización es el proceso por el cual átomos o moléculas, que normalmente son eléctricamente neutros, se convierten en partículas con carga eléctrica, conocidas como iones. Esta transformación ocurre cuando ganan o pierden electrones. Piensen en los electrones como pequeños componentes que orbitan el núcleo de un átomo. El número normal de electrones en un átomo neutro equilibra la carga positiva de los protones en su núcleo.
Cuando un átomo o molécula pierde uno o más electrones, se queda con más carga positiva de los protones, convirtiéndose en un ion con carga positiva. A este tipo de ion lo llamamos catión.
Por otro lado, cuando un átomo o molécula gana un electrón adicional, tiene más carga negativa que positiva, transformándose en un ion con carga negativa. A este tipo de ion lo llamamos anión.
La ionización es uno de los mecanismos principales por los que la radiación, como las partículas cargadas o los rayos X, transfiere su energía a la materia. Es un proceso fundamental en la interacción entre la energía y los átomos.
¿Cómo se Crea la Ionización?
Para que un átomo o molécula cambie su estado electrónico y se ionice, necesita recibir energía. Esta transferencia de energía puede ocurrir de diversas maneras, alterando el equilibrio de electrones. Las formas más comunes de lograr esta transferencia de energía incluyen:
- Colisiones: Una partícula (como otro electrón, ion o incluso un fotón, que es una partícula de luz) choca con el átomo o molécula objetivo con suficiente energía. Esta colisión puede "arrancar" un electrón o añadir uno.
- Reacciones Químicas: En ciertas reacciones, los átomos pueden transferir electrones entre sí, generando iones.
- Absorción de Fotones: Un átomo o molécula puede absorber un fotón (una partícula de luz) con la energía suficiente para liberar un electrón.
Existen procesos más complejos que también pueden generar iones, como la adición química (cuando otras especies se unen a la molécula objetivo) o la desproporción (una reacción donde una molécula se oxida y otra se reduce). Estos mecanismos también implican un reajuste en la distribución de electrones.
Mecanismos de Producción de Iones
Dependiendo de cómo se transfiera la energía, la producción de iones puede describirse a través de diferentes mecanismos:
- Ionización por Captura Electrónica: Aquí es donde se producen iones cargados negativamente. Ocurre cuando un electrón libre choca con un átomo neutro y queda atrapado dentro de su barrera de potencial eléctrico, liberando cualquier exceso de energía.
- Ionización por Colisión de Partículas o Fotones: Los iones cargados positivamente se producen generalmente transfiriendo una cantidad de energía a un electrón ligado en una colisión con partículas cargadas (como iones, electrones o positrones) o con fotones (partículas de luz). La cantidad mínima de energía requerida para este proceso se conoce como energía de ionización. Esta energía es diferente para cada sustancia, lo que significa que distintos elementos o moléculas requieren diferentes "umbrales" de energía para ser ionizados.
El estudio de estas colisiones es de importancia fundamental en física, especialmente en lo que respecta al problema de pocos cuerpos, que es uno de los problemas sin resolver en el campo.
El Efecto Avalancha: Ionización en Gases
Un ejemplo clásico de cómo la ionización puede generar una reacción en cadena es el efecto avalancha, también conocido como descarga de Townsend. Esto ocurre en gases a baja presión cuando se aplica un campo eléctrico lo suficientemente fuerte entre dos electrodos.
Imaginemos que un evento de ionización inicial (quizás causado por radiación) libera un electrón libre. Este electrón se acelera por el campo eléctrico hacia el electrodo positivo (ánodo). Si el campo es lo suficientemente fuerte, el electrón gana suficiente energía entre colisiones con las moléculas de gas como para, en su siguiente colisión, liberar otro electrón. Ahora tenemos dos electrones libres.

Estos dos electrones libres, a su vez, son acelerados y colisionan con otras moléculas, liberando aún más electrones en cada impacto. Este es un efecto de cascada: cada colisión ionizante produce el electrón original (el que colisionó) y el electrón liberado, duplicando el número de electrones libres en cada "generación".
Mientras tanto, los iones positivos creados en estas colisiones se mueven hacia el electrodo negativo (cátodo). Esta reacción en cadena de generación de electrones solo se mantiene si los electrones libres ganan suficiente energía entre colisiones para causar la ionización por impacto. Esencialmente, es una avalancha de ionización impulsada por el campo eléctrico.
Ionización Adiabática y Eficiencia
Otro concepto es la ionización adiabática. Esta es una forma de ionización en la que un electrón es removido o añadido a un átomo o molécula que se encuentra en su estado de energía más bajo, resultando en la formación de un ion que también se encuentra en su estado de energía más bajo.
La eficiencia de ionización es una medida de cuán efectivo es un proceso de ionización. Se define como la relación entre el número de iones formados y el número de electrones o fotones que se utilizaron para intentar la ionización. Una mayor eficiencia significa que se obtienen más iones por cada partícula o fotón invertido.
La Energía de Ionización y la Tabla Periódica
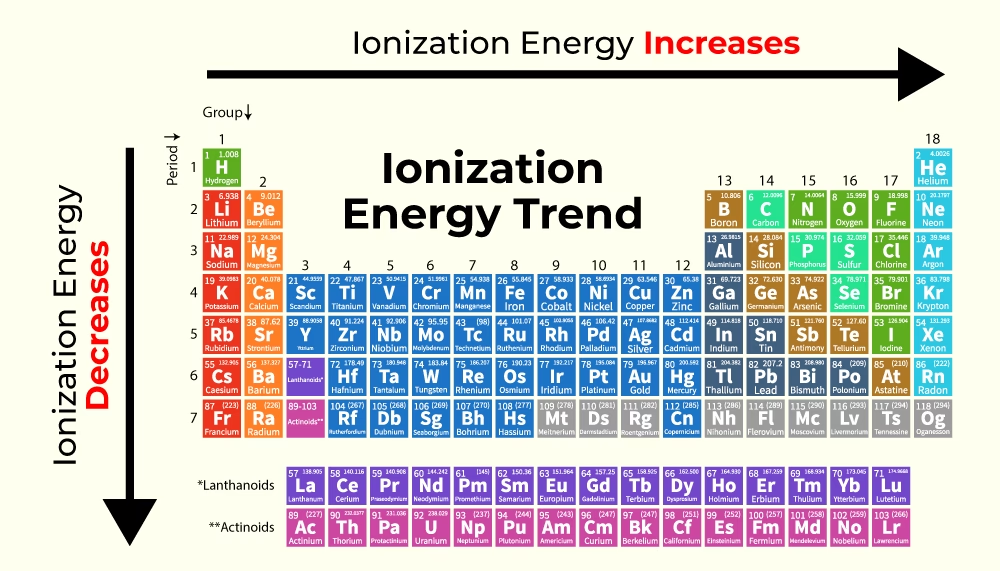
La energía de ionización de los átomos neutros presenta patrones periódicos que son muy útiles para entender el comportamiento de los elementos. Al observar cómo varía la energía de ionización a lo largo de la tabla periódica, podemos inferir la forma en que los electrones se organizan en los orbitales atómicos.
Por ejemplo, la disminución abrupta en el potencial de ionización después de los gases nobles indica la aparición de una nueva capa electrónica en los metales alcalinos. De manera similar, los máximos locales en el gráfico de energía de ionización al moverse de izquierda a derecha en una fila sugieren la presencia de las subcapas s, p, d y f dentro de las capas electrónicas.

Ionización vs. Disociación: Una Diferencia Clave
A veces, se confunden los términos ionización y disociación. Es importante entender la diferencia.
La disociación es simplemente el proceso por el cual una sustancia se separa en partes más pequeñas. Por ejemplo, cuando disolvemos azúcar en agua, las moléculas de azúcar se separan unas de otras y se dispersan en el agua. Sin embargo, cada molécula de azúcar sigue siendo una entidad neutra. No se crean iones en este proceso.
Un caso más sutil es la disolución de sal de mesa (cloruro de sodio, NaCl) en agua. Podría parecer que se ioniza, pero en realidad, los iones de sodio (Na+) y cloruro (Cl-) ya existen dentro de la estructura cristalina de la sal sólida. Cuando la sal se disuelve, estos iones preexistentes simplemente se separan y son rodeados por moléculas de agua. No hay una transferencia o desplazamiento de electrones que ocurra durante la disolución de la sal para crear los iones; los iones ya estaban allí, simplemente unidos en una red.
La ionización, por otro lado, implica la creación de iones a partir de átomos o moléculas neutras mediante la ganancia o pérdida de electrones.
Aquí tienes una tabla simple para comparar:
| Proceso | ¿Se crean iones? | Ejemplo | Cambio de Electrones |
|---|---|---|---|
| Ionización | Sí, a partir de entidades neutras | Gas en un campo eléctrico | Sí (ganancia o pérdida) |
| Disociación (general) | No necesariamente | Azúcar en agua | No |
| Disociación (de sales iónicas) | No (iones ya existen) | Sal en agua | No (solo separación) |
Preguntas Frecuentes sobre Ionización
Aunque es un tema técnico, las preguntas básicas sobre la ionización son bastante sencillas:
- ¿Qué es un ion?
Un ion es un átomo o molécula que ha adquirido una carga eléctrica neta, ya sea positiva (si perdió electrones) o negativa (si ganó electrones), a diferencia de un átomo o molécula neutra que no tiene carga neta. - ¿Cómo se forman los iones?
Los iones se forman cuando un átomo o molécula neutra gana o pierde electrones. Esto generalmente ocurre porque el átomo o molécula recibe suficiente energía a través de colisiones con otras partículas (como electrones o fotones), reacciones químicas o absorción de luz. Esta energía permite que los electrones superen la atracción del núcleo (para ser removidos) o sean capturados (para ser añadidos).
Existen descripciones más avanzadas de la ionización, como las que involucran la mecánica cuántica para fenómenos como la ionización por túnel (donde un electrón pasa a través de una barrera de energía que clásicamente no podría superar) o la ionización multifotónica (donde se absorben varios fotones para ionizar un átomo). También hay estudios sobre la ionización no secuencial y el atrapamiento de población en campos láser intensos, pero estos son conceptos bastante complejos que requieren un conocimiento profundo de física para comprender completamente.
En resumen, la ionización es un proceso científico fundamental que transforma átomos y moléculas neutras en iones cargados mediante la ganancia o pérdida de electrones, impulsado por la transferencia de energía a través de colisiones, reacciones o absorción de luz. Es un concepto clave en química, física y muchas otras áreas de la ciencia, aunque invisible en nuestro día a día.
Si quieres conocer otros artículos parecidos a La Ciencia Oculta: Entendiendo la Ionización puedes visitar la categoría Maquillaje.

