21/10/2016
¡Hola, amantes de la belleza y la ciencia! Hoy vamos a adentrarnos en un tema que, aunque parezca alejado de nuestros labiales y sombras favoritas, es fundamental para entender todo lo que nos rodea: la composición de la materia. Sí, nos pondremos un poco científicas, pero prometo que será un viaje fascinante al corazón mismo de las cosas.

Todo en el universo, desde el aire que respiramos hasta los pigmentos de tu paleta más preciada, está compuesto por elementos. Y la unidad más pequeña e indivisible de un elemento es el átomo. Piensa en los átomos como los ladrillos LEGO fundamentales que construyen todo lo demás. Estos elementos y sus átomos están organizados de forma maravillosa en un gran mapa que quizás recuerdes de tus clases de química: la tabla periódica de los elementos.
En esta tabla, cada elemento tiene un número que lo identifica, llamado número atómico. Pero hoy, nuestro enfoque principal es otro número crucial: la masa atómica. ¿Qué es exactamente y de qué está compuesta?
Los Componentes Esenciales del Átomo
Para entender la masa atómica, primero debemos mirar dentro del átomo. Aunque increíblemente pequeños, los átomos no son unidades simples. Están formados por partículas aún más diminutas:
- Protones
- Neutrones
- Electrones
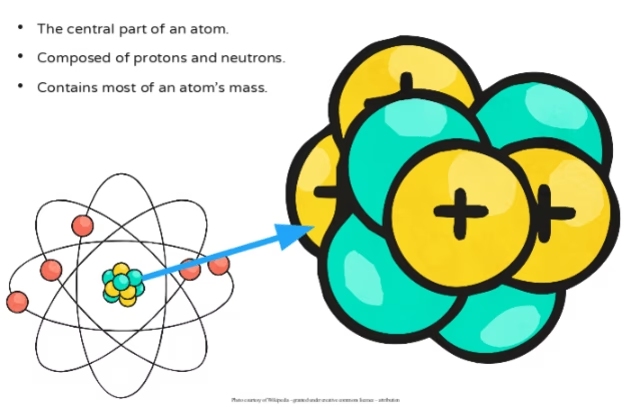
Imagina el átomo como un sistema solar en miniatura. En el centro, tenemos un núcleo denso, similar al sol, y a su alrededor giran los electrones, como planetas en órbita. La mayor parte de la masa del átomo se concentra precisamente en ese núcleo central.
El Corazón Denso: Protones y Neutrones
El núcleo del átomo está formado por dos tipos de partículas: los protones y los neutrones. Ambas son partículas hadrones y son las que aportan la mayor parte de la masa al átomo. Los protones tienen una carga eléctrica positiva, mientras que los neutrones, como su nombre sugiere, no tienen carga (son neutros).
Lo interesante es cómo medimos la masa de estas partículas subatómicas. En lugar de usar gramos, que serían números increíblemente pequeños e imprácticos (¡como 1/167 seguido de muchísimos ceros en el denominador para un protón o neutrón!), usamos una unidad de medida especial para el mundo atómico: la unidad de masa atómica (amu).
La Unidad de Masa Atómica (amu)
La unidad de masa atómica, o amu, fue definida de una manera muy ingeniosa. Se basó en el átomo de carbono más común, el Carbono-12. Este átomo tiene exactamente seis protones y típicamente seis neutrones en su núcleo. Se decidió que la masa de un átomo de Carbono-12 sería exactamente 12 amu. De esta definición se deriva que tanto un protón como un neutrón tienen, cada uno, una masa aproximada de 1 amu. ¡Así de simple y elegante!
Es fascinante pensar cómo se llegó a esta unidad. Definirla en base al Carbono-12 hizo que trabajar con las masas de otros átomos fuera mucho más manejable que intentar usar fracciones diminutas de gramo. Nos permite comparar fácilmente las masas de diferentes átomos.
Los Electrones: Pequeños pero Importantes (para la carga, no para la masa)
Orbitando el núcleo están los electrones. Estas partículas tienen una carga eléctrica negativa y son increíblemente ligeras en comparación con los protones y neutrones. Para ponerlo en perspectiva, la masa de un protón es aproximadamente 1,836 veces mayor que la masa de un electrón. Son tan, tan pequeños en términos de masa que, a la hora de calcular la masa total de un átomo, su contribución es considerada despreciable.
Aunque los electrones son cruciales para las propiedades químicas y las interacciones de los átomos (¡son los que forman los enlaces!), no son los protagonistas cuando hablamos de la masa atómica.
Componiendo la Masa Atómica
Ahora que conocemos a los actores principales (protones, neutrones y electrones) y dónde residen (núcleo vs. órbita), podemos entender qué compone la masa atómica de un átomo individual.
La masa atómica es simplemente la masa total de todas las partículas que componen un átomo. Sin embargo, como mencionamos, la masa de los electrones es tan mínima que prácticamente no afecta el total. Por lo tanto, la masa atómica de un átomo individual se calcula sumando la masa de sus protones y la masa de sus neutrones.
Dado que la masa de un protón es aproximadamente 1 amu y la de un neutrón es aproximadamente 1 amu, la masa atómica de un átomo individual es, en la práctica, igual a la suma del número de protones y el número de neutrones que contiene.
Veamos un ejemplo que se mencionaba en la información: el flúor. Los átomos de flúor típicamente tienen 9 protones y 10 neutrones. Si sumamos el número de protones y neutrones (9 + 10), obtenemos 19. Por lo tanto, la masa atómica de un átomo típico de flúor es de aproximadamente 19 amu.
Es importante no confundir la masa atómica con otros números que aparecen en la tabla periódica:
- Número Atómico: Es el número de protones en el núcleo de un átomo. Este número es único para cada elemento y define de qué elemento se trata.
- Número Másico: Es la suma del número de protones y neutrones en un átomo específico (esencialmente, la masa atómica de un isótopo particular, expresada como un número entero).
- Masa Atómica Promedio: Este es el número que generalmente aparece en la tabla periódica bajo el símbolo del elemento. Representa el promedio ponderado de las masas atómicas de todos los isótopos naturales de un elemento, teniendo en cuenta la abundancia de cada isótopo en la naturaleza. Por ejemplo, la masa atómica promedio del flúor es 18.998 amu, muy cercana a 19 porque el isótopo con 10 neutrones es el más común.
Entonces, cuando hablamos de la composición de la masa atómica de un átomo individual, nos referimos fundamentalmente a la suma de las masas de sus protones y neutrones, ubicados en el núcleo.
Comparando los Componentes
Para visualizar mejor las diferencias entre las partículas subatómicas, aquí tienes una tabla comparativa:
| Partícula | Ubicación en el Átomo | Carga Eléctrica | Masa (en amu) |
|---|---|---|---|
| Protón | Núcleo | Positiva (+1) | ~1 |
| Neutrón | Núcleo | Neutra (0) | ~1 |
| Electrón | Orbitando el Núcleo | Negativa (-1) | ~0 (despreciable) |
Esta tabla resalta por qué los protones y neutrones son los que determinan la masa atómica de un átomo individual: ¡son las partículas "pesadas" del átomo!
Profundizando un Poco Más
La idea de que la masa atómica se concentra casi por completo en el núcleo fue un descubrimiento crucial en la física. Antes de esto, se pensaba que la masa y la carga positiva estaban distribuidas uniformemente por todo el átomo. El famoso experimento de la lámina de oro de Rutherford, donde las partículas alfa rebotaban al chocar con los átomos de oro, demostró la existencia de un núcleo pequeño, denso y cargado positivamente, confirmando que la masa del átomo residía principalmente allí.
Entender la composición de la masa atómica nos ayuda a comprender por qué los diferentes elementos tienen propiedades diferentes y por qué se organizan como lo hacen en la tabla periódica. La cantidad de protones define el elemento (y su número atómico), mientras que la cantidad de neutrones (junto con los protones) determina su masa atómica y puede dar lugar a diferentes isótopos del mismo elemento.
Aunque en nuestro día a día, al elegir un labial o una base, no pensamos directamente en protones y neutrones, es fascinante saber que la estabilidad, el color y las propiedades de los materiales que usamos provienen en última instancia de cómo estos diminutos componentes se organizan en cada átomo y cómo los átomos interactúan entre sí.
La masa atómica es, por lo tanto, una propiedad fundamental de cada átomo, dictada por el número de protones y neutrones en su núcleo. Es un concepto clave en química y física, que nos permite cuantificar y comparar la cantidad de materia en el nivel más básico.
La precisión con la que se mide la masa atómica promedio (con varios decimales, como el 18.998 para el flúor) refleja la sofisticación de la ciencia moderna y la capacidad de determinar la abundancia de los diferentes isótopos de un elemento en la naturaleza. Cada decimal cuenta cuando se trabaja con las cantidades minúsculas del mundo atómico.
En resumen, la masa atómica de un átomo individual es la suma de las masas de sus protones y neutrones. Estos se encuentran en el núcleo y tienen una masa aproximada de 1 amu cada uno. Los electrones, aunque fundamentales, son demasiado ligeros para contribuir significativamente a la masa total.
Preguntas Frecuentes
Aquí respondemos algunas dudas comunes sobre este tema:
¿Qué es exactamente la masa atómica?
Es la masa total de las partículas (protones, neutrones, electrones) que componen un átomo individual. Sin embargo, debido a que los electrones son tan ligeros, en la práctica es la suma de las masas de los protones y neutrones.
¿De qué está compuesto el núcleo de un átomo?
El núcleo, que concentra la mayor parte de la masa del átomo, está compuesto por protones (carga positiva) y neutrones (sin carga).
¿Por qué los electrones no se tienen en cuenta para la masa atómica?
Los electrones tienen una masa extremadamente pequeña en comparación con los protones y neutrones (aproximadamente 1/1836 la masa de un protón). Su contribución a la masa total del átomo es insignificante y se considera despreciable en la mayoría de los cálculos de masa atómica.
¿Qué es una unidad de masa atómica (amu)?
Es una unidad de medida estándar utilizada para expresar las masas de átomos y moléculas. Se define basándose en la masa de un átomo de Carbono-12, al que se le asignan exactamente 12 amu. Un protón y un neutrón tienen cada uno una masa de aproximadamente 1 amu.
¿Cuál es la diferencia entre masa atómica y número atómico?
El número atómico es el número de protones en el núcleo de un átomo y define el elemento. La masa atómica es la suma de las masas de protones y neutrones (principalmente) en un átomo individual.
¿La masa atómica es siempre un número entero?
La masa atómica de un isótopo específico (número másico) es un número entero (suma de protones y neutrones). Sin embargo, la masa atómica real de un átomo individual no es *exactamente* un número entero debido a pequeñas variaciones de masa relacionadas con la energía de enlace. Además, la masa atómica *promedio* que aparece en la tabla periódica es el promedio ponderado de las masas de los isótopos naturales y casi siempre es un número decimal.
Espero que este viaje al interior del átomo haya sido tan esclarecedor para ti como lo es para la ciencia. Entender los componentes básicos de la materia nos da una nueva perspectiva sobre el mundo físico que nos rodea, recordándonos la increíble complejidad que existe incluso en las unidades más pequeñas. ¡Hasta la próxima, con más descubrimientos fascinantes!
Si quieres conocer otros artículos parecidos a Descifrando la Masa Atómica: Sus Componentes puedes visitar la categoría Maquillaje.
