07/03/2019
Las proteínas son, sin duda, las moléculas más complejas y sofisticadas que conocemos desde un punto de vista químico y funcional. Su estructura y química han sido perfeccionadas a lo largo de miles de millones de años de evolución. Comprender de qué están hechas y cómo adquieren su forma es fundamental para desentrañar sus innumerables funciones en las células y organismos. Desde enzimas que catalizan reacciones hasta componentes estructurales que dan soporte, las proteínas son los caballos de batalla de la vida.

En este artículo, exploraremos los componentes básicos de las proteínas, cómo se unen, los diferentes niveles de organización que forman y cómo su forma tridimensional única determina su función. También abordaremos las fuentes dietéticas de proteínas y la importancia de consumir los tipos correctos de aminoácidos.
Los Bloques de Construcción: Aminoácidos
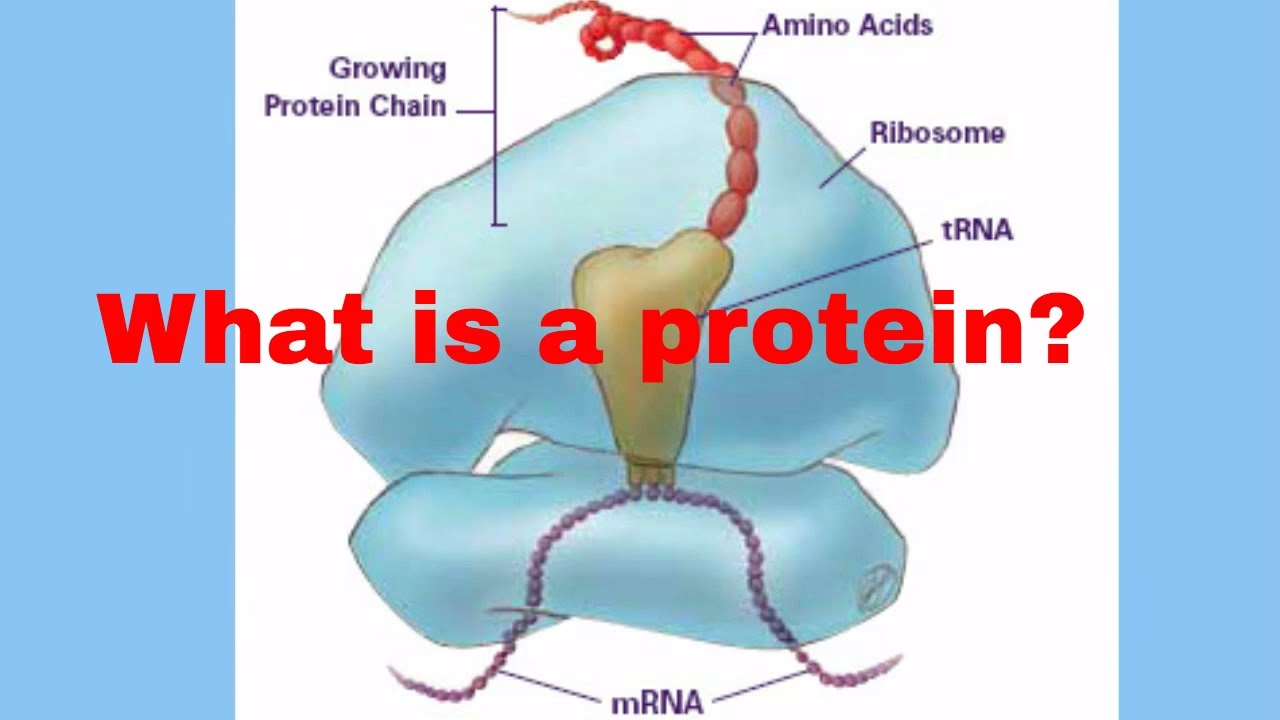
Químicamente, las proteínas son polímeros lineales compuestos por una secuencia específica de unidades más pequeñas llamadas aminoácidos. Existen 20 tipos diferentes de aminoácidos que se encuentran comúnmente en las proteínas, cada uno con propiedades químicas distintas. Estos aminoácidos se unen entre sí mediante un enlace covalente fuerte conocido como enlace peptídico, formando largas cadenas llamadas polipéptidos.
Cada aminoácido tiene una estructura central similar, que incluye un grupo amino, un grupo carboxilo y un átomo de carbono central (carbono alfa). La diferencia entre los 20 aminoácidos radica en su cadena lateral, también conocida como grupo R. Estas cadenas laterales varían enormemente en tamaño, forma, carga eléctrica y polaridad, lo que confiere a cada aminoácido sus propiedades únicas. Algunas cadenas laterales son no polares e hidrofóbicas ("temerosas del agua"), otras son polares o tienen carga positiva o negativa, y algunas son reactivas. Es la secuencia específica de estas cadenas laterales químicamente diversas a lo largo de la cadena polipeptídica la que determina las propiedades y la forma final de la proteína.
Aunque existen cientos de aminoácidos en la naturaleza, solo alrededor de 20 son necesarios para sintetizar todas las proteínas en el cuerpo humano y la mayoría de otras formas de vida. Estos son los que típicamente se refieren al hablar de la composición de las proteínas. Además de estos 20, se han descrito recientemente dos aminoácidos adicionales incorporados a veces en proteínas: la selenocisteína y la pirrolisina. Sin embargo, la pirrolisina no se encuentra en humanos.
Aminoácidos Esenciales y No Esenciales
Desde un punto de vista nutricional, los aminoácidos se clasifican en tres grupos:
- Esenciales: Aquellos que el cuerpo humano no puede sintetizar por sí mismo y deben obtenerse a través de la dieta. Hay 9 aminoácidos esenciales: histidina, isoleucina, leucina, lisina, metionina, fenilalanina, treonina, triptófano y valina.
- No Esenciales: Aquellos que el cuerpo puede sintetizar a partir de otros compuestos.
- Semi-esenciales (o Condicionalmente Esenciales): Aquellos que el cuerpo puede sintetizar, pero en cantidades insuficientes durante ciertos períodos fisiológicos, como el crecimiento rápido (niños, mujeres embarazadas o lactantes) o la recuperación de trauma. Ejemplos incluyen arginina e histidina.
La calidad nutricional de una proteína dietética a menudo se mide por la cantidad y proporción de aminoácidos esenciales que contiene.
Estructura Proteica: Niveles de Organización
La cadena lineal de aminoácidos es solo el comienzo. Las proteínas adquieren su forma tridimensional funcional a través de varios niveles de organización:
- Estructura Primaria: Es simplemente la secuencia lineal y única de aminoácidos en la cadena polipeptídica. Esta secuencia está determinada por la secuencia de nucleótidos en el gen que codifica la proteína. La estructura primaria es crucial porque contiene toda la información necesaria para que la proteína se pliegue correctamente.
- Estructura Secundaria: Se refiere a los patrones de plegamiento locales y regulares de la cadena polipeptídica. Estos patrones se forman principalmente debido a los enlaces de hidrógeno que se establecen entre los átomos del esqueleto peptídico. Las dos estructuras secundarias más comunes son la hélice alfa (α-hélice) y la lámina beta (β-lámina o β-plegada).
- Estructura Terciaria: Describe la organización tridimensional completa de una sola cadena polipeptídica, incluyendo cómo se pliegan las estructuras secundarias (hélices alfa y láminas beta) y cómo interactúan las cadenas laterales de los aminoácidos entre sí. Esta estructura global está estabilizada por diversas interacciones débiles (enlaces de hidrógeno, interacciones iónicas, fuerzas de Van der Waals) y, a veces, por enlaces covalentes fuertes como los puentes disulfuro entre residuos de cisteína.
- Estructura Cuaternaria: Se presenta en proteínas compuestas por dos o más cadenas polipeptídicas separadas (llamadas subunidades proteicas) que se asocian para formar un complejo funcional. La estructura cuaternaria describe la disposición espacial de estas subunidades. Estas subunidades se mantienen unidas por interacciones no covalentes similares a las que estabilizan la estructura terciaria. La hemoglobina, compuesta por cuatro subunidades (dos alfa y dos beta), es un ejemplo clásico.
La estructura tridimensional final de una proteína, o conformación, es generalmente aquella en la que se minimiza la energía libre. El plegamiento proteico está guiado por las interacciones entre los aminoácidos y su entorno acuoso. Las cadenas laterales hidrofóbicas tienden a agruparse en el interior de la proteína, lejos del agua, mientras que las cadenas laterales polares tienden a ubicarse en la superficie, donde pueden interactuar con el agua.
Dominios Proteicos
Las proteínas grandes a menudo están organizadas en unidades estructurales y funcionales distintas llamadas dominios proteicos. Un dominio es una parte de una cadena polipeptídica que se puede plegar de forma independiente en una estructura compacta y estable. Los dominios suelen tener entre 40 y 350 aminoácidos y son las unidades modulares a partir de las cuales se construyen muchas proteínas más grandes. Diferentes dominios dentro de una misma proteína a menudo están asociados con diferentes funciones. Por ejemplo, la proteína cinasa Src tiene dominios SH2 y SH3 con roles reguladores, mientras que otros dominios son responsables de su actividad catalítica como cinasa.
La evolución ha utilizado el "barajado de dominios", donde los segmentos de ADN que codifican dominios se han unido accidentalmente en nuevas combinaciones, dando lugar a nuevas proteínas con funciones novedosas. Algunos dominios, llamados módulos proteicos, han sido particularmente móviles evolutivamente y tienen estructuras versátiles que les permiten integrarse fácilmente en otras proteínas.
El Plegamiento Proteico y las Chaperonas Moleculares
Sorprendentemente, la información para el plegamiento correcto de una proteína a menudo está contenida completamente en su secuencia de aminoácidos. Experimentos de desnaturalización y renaturalización muestran que las proteínas desplegadas pueden recuperar espontáneamente su forma original cuando se eliminan las condiciones desnaturalizantes.
Sin embargo, en el entorno celular abarrotado, el plegamiento proteico a menudo es asistido por proteínas especiales llamadas chaperonas moleculares. Estas chaperonas se unen a cadenas polipeptídicas parcialmente plegadas y ayudan a guiar el proceso de plegamiento por la vía energéticamente más favorable, evitando la formación de agregados proteicos incorrectos. Aunque las chaperonas ayudan, la forma final de la proteína sigue siendo especificada por su secuencia de aminoácidos.
Fuentes Dietéticas de Proteínas
Obtener suficientes proteínas a través de la dieta es crucial para el crecimiento, la reparación celular y el funcionamiento adecuado del cuerpo. Las proteínas se encuentran en una amplia variedad de alimentos.
Generalmente, las fuentes de proteínas se dividen en animales y vegetales:
Fuentes Animales:
- Carnes magras (res, cordero, cerdo, aves)
- Pescado y mariscos
- Huevos
- Productos lácteos (leche, yogur, queso)
Fuentes Vegetales:
- Legumbres y frijoles (lentejas, garbanzos, guisantes partidos, frijoles)
- Frutos secos y semillas
- Tofu y otros productos de soja
- Cereales integrales (en menor proporción que otras fuentes)
- Quinoa, amaranto
Las proteínas de origen animal y algunos vegetales (como la soja, quinoa y amaranto) suelen considerarse proteínas de "alta calidad" porque contienen cantidades significativas de todos los aminoácidos esenciales. Otras proteínas vegetales contienen todos los aminoácidos esenciales, pero la cantidad de uno o dos puede ser baja. Las personas que siguen dietas vegetarianas o veganas estrictas deben asegurarse de consumir una variedad de fuentes de proteínas vegetales a lo largo del día para obtener una mezcla adecuada de todos los aminoácidos esenciales.
Tabla Comparativa de Fuentes Proteicas (Ejemplo General)
| Tipo de Fuente | Ejemplos | Contenido de Aminoácidos Esenciales |
|---|---|---|
| Animal | Carne, pescado, huevos, lácteos | Alto (generalmente "completa") |
| Vegetal (Completa) | Soja, Quinoa, Amaranto | Alto (similar a animal) |
| Vegetal (Incompleta) | Legumbres, frutos secos, cereales (individualmente) | Variable (puede ser bajo en uno o dos esenciales, complementarias entre sí) |
Consumir una variedad de alimentos proteicos a lo largo del día es la mejor manera de asegurar la ingesta adecuada de todos los aminoácidos necesarios.

Ensamblaje de Estructuras Más Grandes
Las proteínas no solo existen como moléculas individuales. Los mismos principios de interacciones no covalentes que permiten a una cadena polipeptídica plegarse también permiten que las proteínas se unan entre sí para formar estructuras más grandes y complejas, como filamentos, ribosomas, cápsides virales y grandes complejos enzimáticos. Cualquier región en la superficie de una proteína que puede interactuar con otra molécula se llama sitio de unión.
Estas grandes estructuras a menudo se construyen a partir del ensamblaje no covalente de muchas moléculas fabricadas por separado que actúan como subunidades. El uso de subunidades más pequeñas para construir estructuras grandes tiene ventajas, como requerir menos información genética y permitir un control más sencillo del ensamblaje y desensamblaje.
Algunas estructuras pueden autoensamblarse espontáneamente a partir de sus componentes purificados en condiciones adecuadas, lo que demuestra que la información para formar la estructura final está contenida en las subunidades mismas. Un ejemplo clásico es el virus del mosaico del tabaco (TMV).
Sin embargo, no todas las estructuras celulares pueden autoensamblarse. Muchas requieren la ayuda de factores de ensamblaje especiales, como enzimas o proteínas andamio, que guían la construcción pero no forman parte de la estructura final. Otros procesos de ensamblaje pueden implicar pasos irreversibles, como la escisión proteolítica, como ocurre en la formación de insulina a partir de proinsulina.
Deficiencia Proteica y su Importancia Clínica
La deficiencia proteica ocurre cuando no se ingiere suficiente proteína en la dieta. Aunque es poco común en países desarrollados con dietas variadas, puede afectar a personas con requerimientos especiales, como ancianos o personas con dietas vegetarianas/veganas estrictas mal planificadas, o en regiones con acceso limitado a alimentos nutritivos.
Los síntomas de la deficiencia proteica pueden incluir:
- Atrofia y pérdida de tejido muscular.
- Edema (acumulación de líquidos).
- Anemia.
- Crecimiento lento (en niños).
La ingesta adecuada de proteínas es vital para mantener la masa muscular a medida que envejecemos (previniendo la sarcopenia) y para funciones corporales esenciales como la producción de neurotransmisores y hormonas.
Además de la deficiencia, los problemas en el metabolismo de los aminoácidos o el plegamiento incorrecto de las proteínas están asociados con diversas enfermedades humanas, como la fenilcetonuria (un error del metabolismo de los aminoácidos) o enfermedades neurodegenerativas como el Alzheimer y las encefalopatías espongiformes transmisibles, donde las proteínas adoptan conformaciones citotóxicas (como las láminas beta anormales en el Alzheimer).
Preguntas Frecuentes
¿Cuántos aminoácidos componen las proteínas?
Las proteínas en la mayoría de los organismos vivos, incluidos los humanos, están compuestas principalmente por 20 tipos diferentes de aminoácidos. Aunque se han descrito algunos aminoácidos adicionales que pueden incorporarse en proteínas en ciertos organismos (como la selenocisteína y la pirrolisina), los 20 son los fundamentales y universales.
¿Qué son los aminoácidos esenciales?
Los aminoácidos esenciales son aquellos que el cuerpo humano no puede sintetizar por sí mismo y, por lo tanto, deben obtenerse necesariamente a través de la dieta para mantener la salud y permitir la síntesis proteica adecuada.
¿La secuencia de aminoácidos afecta la función de la proteína?
Absolutamente. La secuencia específica de aminoácidos (estructura primaria) determina la forma tridimensional única de la proteína (estructuras secundaria, terciaria y cuaternaria). Esta forma es fundamental para la función de la proteína, ya que define sus sitios de unión y cómo interactúa con otras moléculas. Un cambio en incluso un solo aminoácido puede, en algunos casos, alterar drástimensionalmente la estructura y la función de la proteína.
¿Qué son los dominios proteicos?
Los dominios proteicos son unidades estructurales y funcionales compactas dentro de una cadena polipeptídica más grande. Pueden plegarse de forma independiente y a menudo están asociados con funciones específicas. Las proteínas grandes suelen estar compuestas por múltiples dominios.
¿Todas las proteínas se pliegan solas?
Si bien la información para el plegamiento está en la secuencia de aminoácidos, en las células vivas, el proceso a menudo es asistido por chaperonas moleculares. Estas proteínas ayudan a guiar el plegamiento correcto, especialmente en el ambiente celular abarrotado, y previenen la formación de agregados de proteínas mal plegadas.
En resumen, las proteínas son macromoléculas fascinantes construidas a partir de 20 aminoácidos diferentes, cuya secuencia única dicta su compleja estructura tridimensional. Esta forma precisa es lo que les permite llevar a cabo la vasta gama de funciones esenciales para la vida. Desde la digestión hasta la estructura celular y la señalización, las proteínas son actores centrales en cada proceso biológico.
Si quieres conocer otros artículos parecidos a ¿De Qué Están Hechas las Proteínas? puedes visitar la categoría Maquillaje.