11/08/2016
El cuerpo humano es una maravilla de la biología, una máquina extraordinariamente compleja capaz de pensar, moverse y sentir. Pero, ¿de qué está hecho realmente? Si descomponemos la materia que nos compone hasta su nivel más fundamental, encontramos que todo está formado por átomos. Y la cantidad de estos diminutos componentes en una sola persona es simplemente asombrosa.
¿Cuántos Átomos Hay en un Cuerpo Humano?
Tratar de escribir la cantidad exacta de átomos en un cuerpo humano promedio es una tarea casi imposible, ya que el número es inmensamente grande. Para un adulto de aproximadamente 70 kilogramos, la estimación es de alrededor de 7 x 1027 átomos. ¿Qué significa este número? Significa un 7 seguido de 27 ceros. Es una cifra que desafía la comprensión intuitiva:
7,000,000,000,000,000,000,000,000,000
Esta vasta cantidad incluye átomos de muchos elementos diferentes, aunque algunos contribuyen mucho más que otros. Los tres elementos más abundantes, que en conjunto constituyen aproximadamente el 99% de la masa atómica total, son el hidrógeno, el oxígeno y el carbono. El hidrógeno, el elemento más ligero, representa la mayor parte de los átomos, con alrededor de 4.7 x 1027 átomos. El oxígeno le sigue con aproximadamente 1.8 x 1027 átomos, y el carbono contribuye con cerca de 7.0 x 1026 átomos.
Es importante recordar que estos números se refieren a la cantidad de átomos, no al porcentaje del peso corporal. Por peso, el oxígeno es el más abundante debido a que sus átomos son más pesados que los de hidrógeno.
Los Elementos Fundamentales de la Vida
En la naturaleza existen 92 elementos que se dan de forma natural. Sin embargo, la vida en la Tierra se construye a partir de una selección muy limitada de estos. Para los seres vivos, solo unos pocos elementos se encuentran en cantidades significativas. Los elementos presentes en cantidades muy pequeñas (0.01% o menos) se consideran oligoelementos (o elementos traza).
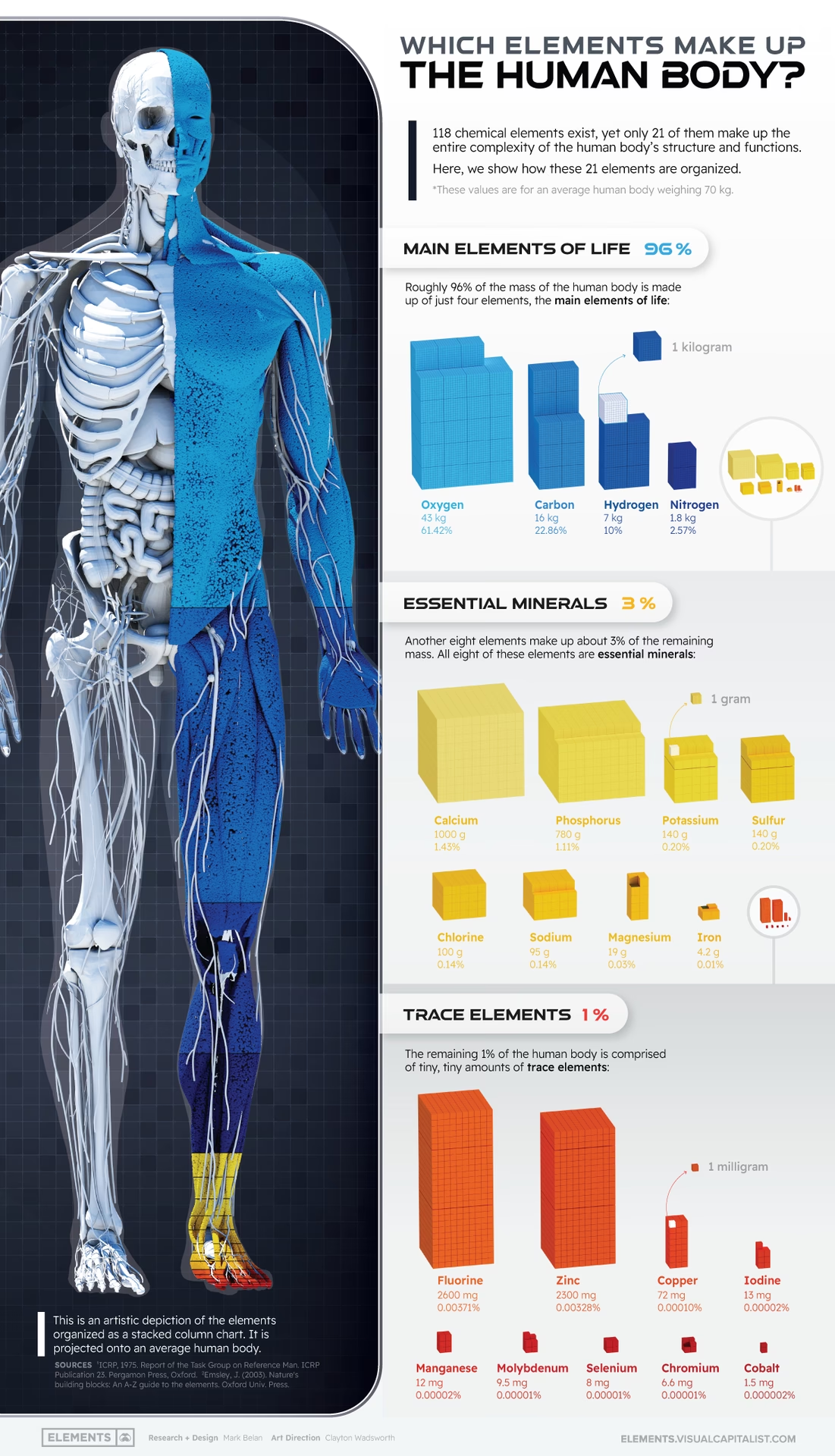
Los cuatro elementos que constituyen la mayor parte de la masa de los organismos vivos (aproximadamente el 96.5% al 96.2% del peso corporal en humanos) son el oxígeno (O), el carbono (C), el hidrógeno (H) y el nitrógeno (N). A menudo se les denomina los cuatro elementos fundamentales de la vida. Aunque el oxígeno y el hidrógeno son componentes principales del agua, que representa más de la mitad de nuestro cuerpo (50-70%), el carbono y el nitrógeno son esenciales para formar las moléculas orgánicas complejas que veremos más adelante.
Otros elementos comunes, aunque en menor proporción que los cuatro principales, incluyen el azufre (S), el fósforo (P), el calcio (Ca) y el potasio (K). Estos, junto con los cuatro grandes, a veces se conocen como los elementos principales o a granel de la vida. La composición elemental de los seres vivos difiere notablemente de la del entorno inorgánico no vivo, como la corteza terrestre o la atmósfera, lo que subraya la química distintiva de la vida.
| Elemento | Símbolo | % aproximado del peso corporal |
|---|---|---|
| Oxígeno | O | 65% |
| Carbono | C | 18.5% |
| Hidrógeno | H | 9.5% |
| Nitrógeno | N | 3.2% |
| Calcio | Ca | 1.5% |
| Fósforo | P | 1.0% |
| Potasio | K | 0.4% |
| Azufre | S | 0.3% |
| Sodio | Na | 0.2% |
| Cloro | Cl | 0.2% |
| Magnesio | Mg | 0.1% |
Además de estos, existen numerosos oligoelementos presentes en cantidades muy pequeñas pero cruciales para diversas funciones biológicas, como el hierro (Fe) en la hemoglobina o el yodo (I) en las hormonas tiroideas.
De Átomos a Moléculas: La Magia de los Enlaces
La vida no está hecha de átomos individuales flotando al azar. La complejidad y la función surgen de la forma en que los átomos se unen para formar moléculas. Un átomo, la partícula más pequeña de un elemento que conserva sus propiedades químicas distintivas, tiene un núcleo central cargado positivamente (compuesto por protones y, generalmente, neutrones) rodeado por una nube de electrones cargados negativamente.
El número de protones define el elemento (número atómico), y en un átomo neutro, el número de electrones es igual al de protones. Son los electrones, particularmente los de la capa más externa (electrones de valencia), los que determinan el comportamiento químico de un átomo y su capacidad para interactuar con otros. La configuración de los electrones en estas capas externas busca la estabilidad, generalmente tratando de alcanzar una capa externa completa, lo que impulsa la formación de enlaces químicos.
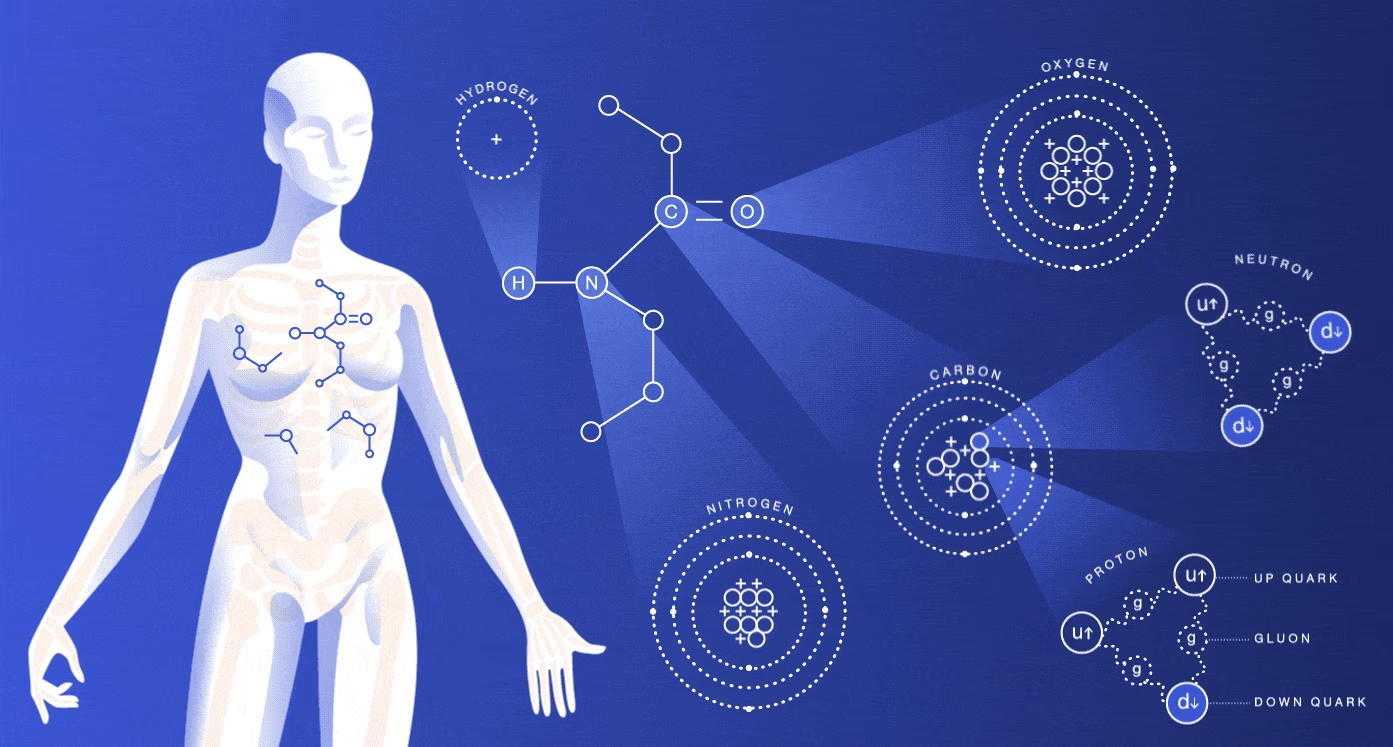
Existen dos tipos principales de enlaces químicos que mantienen unidos a los átomos en las moléculas:
1. Enlaces Iónicos: Se forman por la transferencia de uno o más electrones de un átomo a otro. Esto crea iones, átomos con carga eléctrica (cationes positivos y aniones negativos). La atracción electrostática entre iones de carga opuesta forma el enlace iónico. Un ejemplo clásico es el cloruro de sodio (NaCl), la sal de mesa. En presencia de agua, los enlaces iónicos se debilitan considerablemente debido a la interacción de las moléculas de agua polares con los iones.
2. Enlaces Covalentes: Se forman cuando dos átomos comparten pares de electrones. Esta es la base de la mayoría de las moléculas orgánicas en los seres vivos. Un solo enlace covalente implica compartir un par de electrones, un doble enlace implica compartir dos pares, y así sucesivamente. Los enlaces covalentes son generalmente mucho más fuertes que los enlaces iónicos en entornos acuosos como el interior de una célula y requieren enzimas para romperse o formarse de manera controlada.
La forma en que se comparten los electrones en un enlace covalente puede ser igual (enlace covalente no polar, como en C-H) o desigual (enlace covalente polar, como en O-H o N-H). Los enlaces polares crean dipolos permanentes en la molécula, con una carga parcial positiva en un extremo y una carga parcial negativa en el otro. Estos dipolos son cruciales para las interacciones entre moléculas.
Además de los enlaces covalentes, existen fuerzas intermoleculares o enlaces no covalentes que, aunque individualmente débiles, son fundamentales para la estructura y función biológica cuando actúan en conjunto. Estas incluyen las interacciones iónicas (entre cargas opuestas), los puentes de hidrógeno (una forma especial de interacción polar que involucra un hidrógeno compartido), las fuerzas de Van der Waals (atracciones débiles entre dipolos fluctuantes) y las fuerzas hidrofóbicas (la tendencia de las moléculas no polares a agruparse para minimizar el contacto con el agua).
El Papel Crucial del Agua
El agua (H2O) es la sustancia más abundante en las células, representando alrededor del 70% de su peso. Su omnipresencia y sus propiedades únicas son fundamentales para la vida. La molécula de agua tiene enlaces O-H altamente polares, lo que le confiere una distribución desigual de carga (el oxígeno es parcialmente negativo, los hidrógenos parcialmente positivos). Esta polaridad permite que las moléculas de agua formen puentes de hidrógeno entre sí, donde el hidrógeno de una molécula es atraído por el oxígeno de otra.
Aunque los puentes de hidrógeno son débiles y se rompen y forman constantemente, la red de puentes de hidrógeno entre las moléculas de agua confiere al agua propiedades excepcionales, como un alto punto de ebullición, alta tensión superficial y la capacidad de disolver una gran variedad de sustancias polares y cargadas (sustancias hidrofílicas, o amantes del agua). Las moléculas no polares, como los hidrocarburos, no se disuelven bien en agua y se consideran hidrofóbicas (temerosas del agua).
El agua también juega un papel clave en la química celular al participar en reacciones de condensación (donde se libera una molécula de agua para formar un enlace entre monómeros) y reacciones de hidrólisis (donde se consume una molécula de agua para romper un enlace). Además, el agua puede disociarse ligeramente para formar iones hidronio (H3O+) e iones hidróxido (OH-), lo que establece la base para la escala de pH que mide la acidez o basicidad de una solución. El mantenimiento de un pH cercano a la neutralidad es vital para las células.
Las Grandes Familias de Moléculas Orgánicas
Excluyendo el agua, la mayoría de las moléculas en una célula son compuestos basados en carbono, conocidos como moléculas orgánicas. El carbono es excepcional por su capacidad para formar enlaces covalentes estables consigo mismo y con otros átomos (como H, O, N, S, P), creando cadenas y anillos complejos de tamaño prácticamente ilimitado. Esta versatilidad del carbono es la base de la enorme diversidad molecular de la vida.
Las células contienen miles de tipos diferentes de moléculas orgánicas pequeñas, con pesos moleculares generalmente entre 100 y 1000 Dalton. Estas moléculas pequeñas sirven como bloques de construcción (monómeros) para las grandes macromoléculas de la célula o como fuentes de energía. La mayoría de estas moléculas pequeñas pueden clasificarse en cuatro familias principales:
1. Azúcares (Carbohidratos): Los monosacáridos simples tienen la fórmula general (CH2O)n. La glucosa (C6H12O6) es un monosacárido clave, utilizado como fuente principal de energía. Los monosacáridos pueden unirse mediante reacciones de condensación para formar disacáridos (como la sacarosa) u oligosacáridos y polisacáridos gigantes (como el glucógeno en animales y el almidón en plantas para almacenamiento de energía, o la celulosa y la quitina para soporte estructural). Los polisacáridos pueden ser estructuras ramificadas o lineales.

2. Ácidos Grasos: Tienen una larga cadena hidrocarbonada hidrofóbica y una cabeza de grupo carboxilo (-COOH) hidrofílica. Pueden ser saturados (sin dobles enlaces C-C) o insaturados (con uno o más dobles enlaces, que crean 'codos' en la cadena). Los ácidos grasos se almacenan como reserva energética en forma de triacilgliceroles. Su función más crucial es formar las membranas celulares. Los fosfolípidos, compuestos por dos cadenas de ácidos grasos, un glicerol y un grupo fosfato hidrofílico, son moléculas anfipáticas (con regiones hidrofóbicas e hidrofílicas) que se autoensamblan en bicapas lipídicas, la estructura fundamental de todas las membranas biológicas.
3. Aminoácidos: Son las subunidades que forman las proteínas. Cada aminoácido tiene un grupo amino (-NH2) y un grupo carboxilo (-COOH) unidos a un carbono central (el carbono alfa), más una cadena lateral ('grupo R') que es diferente en cada tipo de aminoácido. Existen 20 tipos comunes de aminoácidos en las proteínas. Se unen mediante enlaces peptídicos en reacciones de condensación para formar cadenas polipeptídicas. La secuencia específica de aminoácidos en una cadena determina cómo se pliega la proteína en su estructura tridimensional única y, por lo tanto, su función.
4. Nucleótidos: Son las subunidades de los ácidos nucleicos, como el ADN (Ácido Desoxirribonucleico) y el ARN (Ácido Ribonucleico), que almacenan y transmiten la información genética. Cada nucleótido consta de una base nitrogenada (adenina, guanina, citosina, timina o uracilo), un azúcar de cinco carbonos (desoxirribosa en ADN, ribosa en ARN) y uno o más grupos fosfato. Los nucleótidos se unen mediante enlaces fosfodiéster para formar las largas cadenas de ADN y ARN.
Macromoléculas: Los Ladrillos de la Vida
Las macromoléculas son los polímeros grandes formados por la unión de muchas subunidades monoméricas. Las proteínas, los ácidos nucleicos y los polisacáridos son las principales macromoléculas en las células. Constituyen la mayor parte de la masa seca de una célula y son responsables de la mayoría de las funciones celulares.
Las proteínas son particularmente diversas y versátiles, realizando miles de funciones: actúan como enzimas (catalizadores biológicos), componentes estructurales (como el citoesqueleto), motores moleculares, transportadores, señales y más. Su función depende críticamente de su estructura tridimensional específica.
La formación de la mayoría de las macromoléculas es un proceso de polimerización escalonada, donde los monómeros se añaden uno a uno en el extremo de una cadena creciente mediante reacciones de condensación. Lo crucial es que, excepto en algunos polisacáridos, los monómeros se añaden en un orden o secuencia específico. Esta secuencia lineal (de aminoácidos en proteínas, de nucleótidos en ADN/ARN) determina la estructura tridimensional y, por tanto, la función de la macromolécula.
Aunque los enlaces covalentes mantienen unida la cadena principal de una macromolécula, las fuerzas no covalentes (enlaces iónicos, puentes de hidrógeno, fuerzas de Van der Waals y fuerzas hidrofóbicas) son las que dictan cómo se pliega la cadena en su forma tridimensional única y estable. Un gran número de interacciones no covalentes, aunque débiles individualmente, pueden sumar una fuerza considerable para estabilizar la conformación de una macromolécula o para permitir que dos macromoléculas se unan de manera específica, como una mano en un guante. Esta especificidad en la unión molecular, mediada por interacciones no covalentes complementarias en sus superficies, es fundamental para todos los procesos biológicos, desde la catálisis enzimática hasta el reconocimiento entre células.
Las macromoléculas a menudo se asocian entre sí mediante interacciones no covalentes para formar complejos supramoleculares más grandes y máquinas celulares intrincadas, como los ribosomas (compuestos de ARN y proteínas) que sintetizan proteínas, o los complejos enzimáticos que realizan vías metabólicas completas.

Elementos Esenciales y Oligoelementos
De los 92 elementos naturales, alrededor del 20-25% se consideran esenciales para la vida, es decir, necesarios para la supervivencia y reproducción de un organismo. La lista exacta varía ligeramente entre especies (por ejemplo, humanos vs plantas).
Los elementos esenciales se clasifican a menudo en macronutrientes y micronutrientes (oligoelementos). Los macronutrientes se requieren en cantidades relativamente grandes e incluyen a los cuatro principales (O, C, H, N), además de P, S, K, Ca, Mg. Los micronutrientes se requieren en cantidades muy pequeñas (trazas), pero son igualmente vitales para diversas funciones enzimáticas y estructurales. Ejemplos en humanos incluyen hierro (Fe), zinc (Zn), cobre (Cu), manganeso (Mn), yodo (I), selenio (Se), entre otros.
La ausencia o deficiencia de cualquiera de estos elementos esenciales, incluso los oligoelementos, puede tener consecuencias graves para la salud y el desarrollo de un organismo, destacando la interconexión de la vida con la química fundamental de la materia.
Preguntas Frecuentes
¿Cuántos átomos hay en el cuerpo humano?
Se estima que hay aproximadamente 7 x 1027 átomos en un adulto promedio de 70 kg.
¿Cuáles son los 4 átomos que componen la mayor parte del cuerpo humano?
Los cuatro elementos que constituyen la mayor parte de la masa del cuerpo humano son el oxígeno (O), el carbono (C), el hidrógeno (H) y el nitrógeno (N). Juntos representan alrededor del 96% del peso corporal.
¿De qué átomos están hechas las células humanas?
Las células humanas están hechas de moléculas, que a su vez están compuestas principalmente por átomos de oxígeno, carbono, hidrógeno y nitrógeno, así como átomos de otros elementos esenciales como fósforo, azufre, potasio, calcio y diversos oligoelementos.
¿Qué son los 4 "átomos de la vida"?
Los 4 "átomos de la vida" se refieren comúnmente a los cuatro elementos más abundantes en todos los seres vivos: carbono (C), hidrógeno (H), oxígeno (O) y nitrógeno (N). Estos forman la base de las principales moléculas orgánicas que componen los organismos.
En conclusión, el cuerpo humano es una estructura increíblemente compleja construida a partir de una cantidad inimaginable de átomos. Estos átomos, principalmente de solo cuatro elementos, se unen mediante enlaces químicos para formar una vasta diversidad de moléculas pequeñas y grandes, que a su vez se organizan en estructuras y llevan a cabo las funciones que definen la vida tal como la conocemos. Es un recordatorio humillante de que, a pesar de nuestra complejidad, estamos intrínsecamente conectados con la química fundamental del universo.
Si quieres conocer otros artículos parecidos a Tu Cuerpo: Un Universo de Átomos puedes visitar la categoría Maquillaje.
