27/05/2019
Las proteínas son verdaderas maravillas moleculares, esenciales para prácticamente todas las funciones de la vida. Son los caballos de batalla de la célula, realizando una vasta gama de tareas que van desde catalizar reacciones químicas hasta formar estructuras de soporte. Pero, ¿cómo logran estas moléculas realizar trabajos tan diversos y complejos? La respuesta reside en su intrincada estructura tridimensional, la cual está dictada por su composición y organización en diferentes niveles.

Para entender la función de una proteína, primero debemos comprender cómo está construida, pieza a pieza, desde sus componentes más básicos hasta su forma final y funcional. Es un proceso de ensamblaje fascinante que determina cada aspecto de su comportamiento.
Los Bloques Constructores: Aminoácidos y Enlaces Peptídicos
En el corazón de toda proteína se encuentran los aminoácidos. Piensa en ellos como los ladrillos moleculares. Son pequeñas moléculas orgánicas que comparten una estructura central común: un átomo de carbono central (llamado carbono alfa) unido a cuatro componentes distintos: un grupo amino (NH₂), un grupo carboxilo (COOH), un átomo de hidrógeno y, lo más importante, un componente variable conocido como cadena lateral o grupo R. Es esta cadena lateral la que confiere a cada aminoácido sus propiedades químicas únicas.
Existen veinte tipos diferentes de aminoácidos que se utilizan comúnmente en la construcción de proteínas. Cada uno posee una cadena lateral distinta, lo que les otorga diferentes características químicas. Algunas cadenas laterales son no polares (hidrofóbicas, es decir, 'temen' al agua), otras tienen cargas positivas o negativas (son iónicas), y otras más son polares pero sin carga neta (hidrofílicas, es decir, 'aman' el agua). La química de estas cadenas laterales es fundamental, ya que determinará cómo interactuarán entre sí y con su entorno, influyendo directamente en la forma final de la proteína.
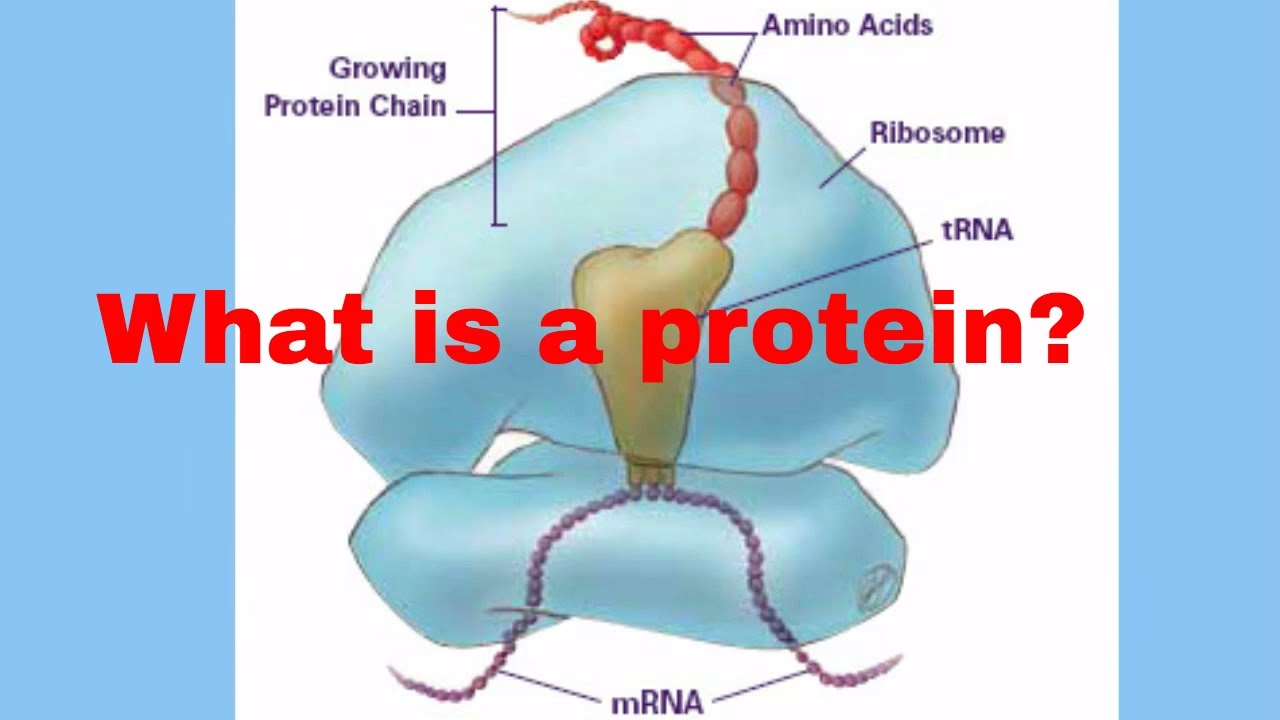
Dentro de una proteína, los aminoácidos se unen en una secuencia lineal específica, como cuentas en un collar. Esta unión se realiza mediante un tipo especial de enlace químico llamado enlace peptídico. Este enlace se forma entre el grupo carboxilo de un aminoácido y el grupo amino del siguiente, liberando una molécula de agua en el proceso. La cadena larga y lineal de aminoácidos unidos por enlaces peptídicos se conoce como polipéptido.
Los Niveles de Organización Proteica
La estructura de una proteína no es estática ni simple. Se describe convencionalmente en cuatro niveles jerárquicos de organización, cada uno construyendo sobre el anterior para definir la forma tridimensional final y funcional de la molécula. Estos niveles son:
- Estructura Primaria
- Estructura Secundaria
- Estructura Terciaria
- Estructura Cuaternaria
Exploremos cada uno de ellos en detalle.
Estructura Primaria (1˚): La Secuencia Lineal
La estructura primaria de una proteína es simplemente la secuencia lineal específica de aminoácidos que la componen. Esta secuencia se determina genéticamente y se lee convencionalmente desde el extremo amino (N-terminal, donde se encuentra el grupo amino libre del primer aminoácido) hasta el extremo carboxilo (C-terminal, donde se encuentra el grupo carboxilo libre del último aminoácido).
Esta secuencia, aparentemente simple, es la base de todo. Es la información codificada en la estructura primaria la que, bajo las condiciones adecuadas, dicta cómo se plegará la proteína en sus niveles superiores de organización. Un solo cambio en un aminoácido de la secuencia puede tener consecuencias drásticas en la estructura y función de la proteína, como ocurre en enfermedades genéticas.
Estructura Secundaria (2˚): Hélices y Láminas
Mientras que la estructura primaria define la secuencia, la estructura secundaria describe los patrones de plegamiento locales y regulares que se forman en segmentos específicos de la cadena polipeptídica. Estos patrones están estabilizados principalmente por puentes de hidrógeno que se forman entre los átomos del esqueleto peptídico (el nitrógeno del grupo amino y el oxígeno del grupo carboxilo de diferentes aminoácidos), no involucrando las cadenas laterales en su formación principal.
Los dos elementos de estructura secundaria más comunes y estables son la hélice alfa (α-hélice) y la lámina beta (β-lámina).
La Hélice Alfa (α-hélice)
La hélice alfa es una estructura en espiral, similar a un muelle. En una α-hélice típica, la cadena polipeptídica se enrolla hacia la derecha. Cada vuelta de la hélice contiene aproximadamente 3.6 residuos de aminoácido y la hélice se eleva unos 5.4 Angstroms por vuelta. La estabilidad de la hélice alfa proviene de los puentes de hidrógeno que se forman entre el grupo C=O de un aminoácido (residuo i) y el grupo N-H de un aminoácido ubicado cuatro posiciones más adelante en la secuencia (residuo i+4). Estos puentes de hidrógeno se orientan casi paralelos al eje de la hélice.
Algunos aminoácidos tienen mayor propensión a formar hélices alfa (como Alanina, Ácido Glutámico, Leucina y Metionina), mientras que otros, como la Prolina, introducen un quiebre o codo en la hélice debido a la rigidez de su estructura cíclica. La hélice alfa también posee un dipolo neto, con el extremo N-terminal ligeramente positivo y el C-terminal ligeramente negativo.
La Lámina Beta (β-lámina)
La lámina beta, también conocida como lámina plegada beta, consiste en segmentos de la cadena polipeptídica casi extendidos, llamados hebras beta (β-hebras). Estas hebras adyacentes se alinean lado a lado y se conectan mediante puentes de hidrógeno entre los átomos del esqueleto peptídico de hebras vecinas. A diferencia de la hélice alfa, los puentes de hidrógeno en las láminas beta son perpendiculares a la dirección de las hebras.

Las hebras beta pueden correr en la misma dirección (lámina beta paralela), en direcciones opuestas (lámina beta antiparalela) o una mezcla de ambas (lámina beta mixta). Las láminas beta son estructuras plegadas, no planas, con los carbonos alfa alternando por encima y por debajo del plano promedio de la lámina. Aunque las hebras individuales tienen un ligero giro a la derecha, la lámina beta en conjunto suele tener un giro a la izquierda. Las cadenas laterales en una hebra beta se proyectan alternativamente por encima y por debajo del plano de la lámina, creando superficies distintas.
Giros Beta y Lazos
Además de hélices y láminas, existen otros elementos de estructura secundaria, como los giros beta (o beta turns) y los lazos (loops) o espirales aleatorias (random coils). Los giros beta son giros cortos (generalmente de 4 residuos) que permiten a la cadena polipeptídica cambiar bruscamente de dirección, a menudo conectando dos hebras beta antiparalelas (formando una 'horquilla beta' o beta hairpin). Suelen involucrar puentes de hidrógeno entre el residuo i y el i+3 y con frecuencia contienen aminoácidos como Glicina (por su flexibilidad) y Prolina (por su capacidad de inducir codos).
Los lazos o espirales aleatorias son regiones de la cadena polipeptídica que no adoptan una estructura secundaria regular (hélice o lámina). Suelen encontrarse en la superficie de las proteínas globulares, expuestos al solvente, y a menudo contienen aminoácidos polares o cargados. Aunque carecen de estructura regular, no son "aleatorios" en el sentido de que su conformación suele ser específica para la proteína y a menudo desempeñan roles funcionales importantes, como sitios de unión para otras moléculas.
Estructura Terciaria (3˚): La Forma 3D Final
La estructura terciaria se refiere a la conformación tridimensional completa y global de una única cadena polipeptídica. Es el resultado del plegamiento de los elementos de estructura secundaria (hélices, láminas, giros, lazos) y su disposición espacial final. Esta forma compacta y única es lo que permite a la proteína llevar a cabo su función biológica.
La estructura terciaria está estabilizada por una variedad de interacciones entre las cadenas laterales de los aminoácidos, que pueden estar distantes en la secuencia primaria pero se acercan en el espacio tridimensional. Estas interacciones incluyen:
- Interacciones hidrofóbicas: Las cadenas laterales no polares (hidrofóbicas) tienden a agruparse en el interior de la proteína, lejos del entorno acuoso del citoplasma, minimizando su contacto con el agua. Este 'efecto hidrofóbico' es una fuerza impulsora principal del plegamiento proteico.
- Puentes de hidrógeno: Se forman entre cadenas laterales polares sin carga o entre cadenas laterales y átomos del esqueleto peptídico.
- Interacciones iónicas (puentes salinos): Se forman entre cadenas laterales con cargas opuestas (ácidas con carga negativa y básicas con carga positiva).
- Fuerzas de van der Waals: Interacciones débiles de corto alcance entre átomos cercanos.
- Puentes disulfuro: Son enlaces covalentes fuertes que se forman entre los átomos de azufre de dos residuos de Cisteína. Estos enlaces aportan una gran estabilidad a la estructura terciaria, aunque son menos comunes en el interior de las células debido al ambiente reductor.
El proceso de plegamiento proteico es complejo y generalmente conduce a la conformación más energéticamente favorable. Aunque la información para el plegamiento está contenida en la estructura primaria (la secuencia de aminoácidos), a menudo este proceso es asistido en la célula por proteínas chaperonas que ayudan a prevenir el plegamiento incorrecto.
Una proteína que se ha plegado correctamente en su forma funcional se dice que está en su estado nativo. El plegamiento incorrecto puede llevar a la formación de proteínas inactivas o, en algunos casos, a agregados tóxicos que están implicados en diversas enfermedades (como el Alzheimer, el Parkinson o las enfermedades priónicas).
Estructura Cuaternaria (4˚): El Ensamblaje de Subunidades
Algunas proteínas son funcionales como una única cadena polipeptídica plegada (estructura terciaria). Sin embargo, muchas otras proteínas consisten en múltiples cadenas polipeptídicas (llamadas subunidades) que se asocian para formar un complejo macromolecular funcional. La estructura cuaternaria describe la disposición espacial y la organización de estas múltiples subunidades en un complejo proteico.
Las subunidades pueden ser idénticas o diferentes. Las proteínas con dos subunidades se llaman dímeros, con tres trímeros, con cuatro tetrámeros, y así sucesivamente (oligómeros). Las subunidades en una estructura cuaternaria se mantienen unidas por el mismo tipo de interacciones no covalentes que estabilizan la estructura terciaria (interacciones hidrofóbicas, puentes de hidrógeno, interacciones iónicas). En algunos casos, también pueden existir puentes disulfuro entre subunidades.
La estructura cuaternaria es crucial para la función de muchas proteínas, especialmente aquellas que exhiben cooperatividad (donde la unión de una molécula a una subunidad afecta la afinidad de otras subunidades por esa molécula, como la hemoglobina que transporta oxígeno) o alosterismo (donde la unión de una molécula a un sitio regula la actividad en otro sitio distante).
Visualizando lo Invisible
Dado que las proteínas son demasiado pequeñas para ser vistas directamente, incluso con microscopios potentes, los científicos utilizan métodos indirectos para determinar sus estructuras tridimensionales. Las técnicas más comunes incluyen la cristalografía de rayos X (donde se analizan los patrones de difracción de rayos X que pasan a través de cristales de proteína purificada) y la espectroscopia de resonancia magnética nuclear (RMN), especialmente útil para estudiar proteínas en solución.
Estas técnicas han revelado la asombrosa diversidad y complejidad de las estructuras proteicas, permitiendo a los científicos comprender mejor cómo estas moléculas llevan a cabo las funciones vitales.
Preguntas Frecuentes sobre la Estructura Proteica
- ¿De qué están hechas las proteínas?
- Las proteínas están hechas de unidades más pequeñas llamadas aminoácidos, unidos entre sí por enlaces peptídicos para formar largas cadenas polipeptídicas.
- ¿Cuántos tipos de aminoácidos hay en las proteínas?
- Hay veinte tipos estándar de aminoácidos que se encuentran comúnmente en las proteínas.
- ¿Cuáles son las 'partes' o niveles de estructura de una proteína?
- Aunque a veces se mencionan tres niveles principales (primaria, secundaria y terciaria), la descripción más completa incluye cuatro niveles: estructura primaria (secuencia de aminoácidos), estructura secundaria (plegamientos locales como hélices alfa y láminas beta), estructura terciaria (la forma 3D global de una cadena polipeptídica) y estructura cuaternaria (la organización de múltiples cadenas polipeptídicas en un complejo funcional).
- ¿Qué determina la forma final de una proteína?
- La forma final y funcional de una proteína está determinada principalmente por su secuencia de aminoácidos (estructura primaria), que dicta cómo se plegará a través de interacciones entre las cadenas laterales de los aminoácidos y el esqueleto peptídico.
- ¿Por qué es importante la forma 3D de una proteína?
- La forma tridimensional específica de una proteína es crucial para su función. Permite que la proteína interactúe selectivamente con otras moléculas y realice su trabajo específico en la célula.
- ¿Pueden las proteínas plegarse incorrectamente?
- Sí, las proteínas pueden plegarse de manera incorrecta, lo que generalmente resulta en una proteína inactiva o, en algunos casos, puede llevar a enfermedades.
Si quieres conocer otros artículos parecidos a La Arquitectura Fascinante de las Proteínas puedes visitar la categoría Maquillaje.