31/07/2021
El tejido conectivo es uno de los tipos de tejido básicos del cuerpo. Como su nombre indica, el "tejido conectivo" se refiere a varios tejidos corporales que conectan, soportan y ayudan a unir otros tejidos. Aunque los diversos tejidos conectivos del cuerpo son diversos, comparten numerosas características estructurales y funcionales. El tejido conectivo se puede dividir en dos categorías principales: tejido conectivo propiamente dicho y tejido conectivo especializado.
Una característica definitoria y crucial del tejido conectivo, y de muchos otros tejidos en el cuerpo, es la presencia de la matriz extracelular. Esta matriz es un espacio no celular, predominantemente lleno de una intrincada red de macromoléculas que son secretadas localmente por las células y ensambladas en un entramado organizado. La matriz extracelular no es simplemente un relleno inerte; desempeña un papel activo y complejo en la regulación del comportamiento celular, influyendo en su supervivencia, desarrollo, migración, proliferación, forma y función. En los tejidos conectivos, la matriz extracelular es frecuentemente más abundante que las células que rodea y determina sus propiedades físicas.
¿De Qué Está Compuesta la Matriz Extracelular?
La matriz extracelular está compuesta principalmente por dos clases de macromoléculas, aunque su composición precisa varía enormemente entre los diferentes tejidos, dando lugar a una asombrosa diversidad de formas adaptadas a los requisitos funcionales específicos.
Componentes Principales de la Matriz
Las dos clases principales de macromoléculas extracelulares que constituyen la matriz son:
- Cadenas de polisacáridos de la clase llamada glicosaminoglicanos (GAGs), que generalmente se encuentran unidas covalentemente a proteínas en forma de proteoglicanos.
- Proteínas fibrosas, incluyendo colágeno, elastina, fibronectina y laminina, que tienen funciones tanto estructurales como adhesivas.
Los proteoglicanos en el tejido conectivo forman una “sustancia fundamental” altamente hidratada, similar a un gel, en la que están incrustadas las proteínas fibrosas.
Sustancia Fundamental: El Gel que lo Une Todo
Los glicosaminoglicanos (GAGs) son cadenas de polisacáridos no ramificadas compuestas por unidades de disacáridos repetidas. Son altamente negativos debido a la presencia de grupos sulfato o carboxilo. Esta alta densidad de carga negativa atrae una nube de cationes, especialmente Na+, que son osmóticamente activos, lo que provoca que grandes cantidades de agua sean absorbidas por la matriz. Esto crea una presión de hinchazón, o turgencia, que permite a la matriz resistir las fuerzas de compresión. El cartílago, por ejemplo, soporta enormes presiones gracias a esta propiedad.
Hay cuatro grupos principales de GAGs: hialuronano, condroitín sulfato y dermatán sulfato, heparán sulfato y queratán sulfato. El hialuronano (también llamado ácido hialurónico o hialuronato) es el más simple de los GAGs; se encuentra en todos los tejidos y fluidos, y es especialmente abundante en embriones tempranos. A diferencia de otros GAGs, no está sulfatado, sus unidades de disacáridos son idénticas, su cadena es enorme y no está generalmente unida a una proteína central. Se sintetiza directamente desde la superficie celular y se cree que facilita la migración celular durante la morfogénesis y reparación tisular.
Excepto el hialuronano, todos los GAGs se encuentran unidos covalentemente a proteínas en forma de proteoglicanos. Estos se componen de una proteína central (core protein) con cadenas de GAGs unidas. Los proteoglicanos pueden ser enormes, como el agrecano (componente principal del cartílago) con más de 100 cadenas de GAGs, o más pequeños, como la decorina con una sola cadena de GAG. Los proteoglicanos regulan las actividades de proteínas secretadas, como factores de crecimiento, uniéndolos y controlando su disponibilidad y función. También pueden servir como tamices selectivos para regular el tráfico de moléculas y células.
Proteínas Fibrosas: La Estructura y Resiliencia
Las proteínas fibrosas son esenciales para la integridad estructural de la matriz.
Colágeno: La Proteína Más Abundante
Los colágenos son una familia de proteínas fibrosas que constituyen aproximadamente el 20-25% del contenido proteico de los humanos, siendo las proteínas más abundantes en mamíferos (25% de la masa proteica total en piel y hueso). La característica principal de una molécula típica de colágeno es su estructura helicoidal triple-helicoidal larga y rígida. Son muy ricas en prolina y glicina, aminoácidos clave para la formación de la triple hélice.
Existen numerosos tipos distintos de cadenas α de colágeno, que se combinan para formar diferentes tipos de moléculas de colágeno (se han encontrado alrededor de 20 tipos). Los tipos principales en tejidos conectivos son I, II, III, V y XI, siendo el tipo I el principal en piel y hueso. Estos son colágenos fibrilares o formadores de fibrilas, que se ensamblan en polímeros de orden superior llamados fibrilas de colágeno (10-300 nm de diámetro) y luego en haces más grandes llamados fibras de colágeno (visibles con microscopio óptico). Las fibrilas de colágeno resisten las fuerzas de estiramiento o tensión.
Otros tipos, como el IX y XII, son colágenos asociados a fibrilas que decoran la superficie de las fibrilas y se cree que las unen entre sí y a otros componentes de la matriz. Los tipos IV y VII son colágenos formadores de red; el tipo IV forma una red en forma de lámina que constituye una parte importante de las láminas basales, mientras que el tipo VII forma fibrilas de anclaje que ayudan a unir las láminas basales al tejido conectivo subyacente.
La síntesis de colágeno es un proceso complejo que implica la hidroxilación de prolina y lisina (requiere Vitamina C), la formación de la triple hélice de procolágeno dentro de la célula, y la posterior escisión de propéptidos y el autoensamblaje en fibrilas en el espacio extracelular. Las fibrilas se refuerzan mediante entrecruzamientos covalentes.
Elastina: La Capacidad de Retorno
Muchos tejidos (piel, vasos sanguíneos, pulmones) necesitan ser fuertes y elásticos. Una red de fibras elásticas les da la resiliencia necesaria para recuperarse después de un estiramiento transitorio. Las fibras elásticas son mucho más extensibles que el colágeno. Su componente principal es la elastina, una proteína altamente hidrofóbica, rica en prolina y glicina, que contiene hidroxiprolina pero no hidroxilisina.
Las moléculas de tropoelastina secretadas se entrecruzan extensamente en el espacio extracelular para formar una red de fibras y láminas de elastina. La elastina se compone de segmentos hidrofóbicos (responsables de la elasticidad) y segmentos ricos en alanina y lisina (forman entrecruzamientos). Las fibras elásticas no son solo elastina; un núcleo de elastina está cubierto por una vaina de microfibrilas compuestas por glicoproteínas, incluida la fibrilina, esencial para la integridad de las fibras elásticas. Mutaciones en el gen de la fibrilina causan el síndrome de Marfan, una enfermedad genética que afecta tejidos ricos en fibras elásticas.
Fibronectina: Adhesión y Migración
La matriz extracelular contiene otras proteínas importantes con múltiples dominios de unión. La fibronectina es una gran glicoproteína encontrada en todos los vertebrados. Es un dímero con dominios funcionales distintos que se unen a colágeno, heparina y receptores celulares específicos (integrinas) a través de secuencias como la RGD (Arg-Gly-Asp). Existe como fibronectina plasmática soluble (en sangre y fluidos corporales) y formas insolubles que se ensamblan en la superficie celular para formar fibrilas de fibronectina en la matriz. La formación de estas fibrilas requiere la tensión ejercida por la célula a través del citoesqueleto de actina y las integrinas. La fibronectina es importante para la adhesión celular a la matriz y para guiar la migración celular, especialmente durante el desarrollo embrionario y la curación de heridas.
Laminina: El Andamio de las Láminas Basales
Las lamininas son grandes glicoproteínas que se encuentran en las láminas basales. Tienen forma de cruz asimétrica, compuesta por tres cadenas polipeptídicas (α, β, γ). Al igual que la fibronectina, tienen múltiples dominios de unión que les permiten unirse a otros componentes de la lámina basal (como perlecan y nidogen) y a receptores celulares (integrinas, distroglicano). Las lamininas pueden autoensamblarse en estructuras similares a láminas y son cruciales para la formación y función de las láminas basales.

Organización y Dinámica de la Matriz
La organización de la matriz extracelular no es aleatoria; las células que la producen también ayudan a organizarla. Por ejemplo, los fibroblastos interactúan mecánicamente con el colágeno que han secretado, arrastrándolo y compactándolo en láminas o cables. Esta tensión celular influye en la alineación de las fibrilas de colágeno, creando estructuras ordenadas como las que se ven en los tendones o en la disposición tipo contrachapado del colágeno en el hueso o la córnea. Las integrinas, proteínas de membrana, son clave en esta interacción bidireccional entre el citoesqueleto intracelular y la matriz extracelular.
La matriz extracelular no es estática; se degrada y resintetiza continuamente, aunque la velocidad de renovación varía enormemente entre tejidos (rápida en la curación de heridas, muy lenta en el hueso). La degradación controlada de componentes de la matriz es crucial para procesos como la migración celular (por ejemplo, durante el desarrollo, la respuesta inmune o la metástasis del cáncer), la remodelación tisular y la curación. Esta degradación es llevada a cabo por enzimas proteolíticas secretadas localmente por las células, como las metaloproteasas de matriz y las serina proteasas. La actividad de estas enzimas está estrictamente regulada por mecanismos como la activación local, la unión a receptores de superficie celular y la secreción de inhibidores específicos (TIMPs, serpinas).
Matrices Especializadas: Cartílago y Hueso
Si bien la matriz extracelular es un tema general, su composición y organización varían drásticamente en tejidos especializados como el cartílago y el hueso, reflejando sus funciones únicas.
Matriz del Cartílago
El cartílago es un tejido conectivo elástico especializado. Su matriz extracelular es responsable de sus propiedades mecánicas y está compuesta principalmente por colágeno tipo II y proteoglicanos. Los condrocitos (células del cartílago) secretan esta matriz rica en proteoglicanos, lo que permite al tejido absorber agua y le confiere elasticidad y resistencia a la compresión. La estructura molecular de la matriz del cartílago hialino, como el cartílago articular, se asemeja a un hidrogel. La fase fluida (agua con iones) y la fase sólida (fibras de colágeno con proteoglicanos interactuando) le dan un comportamiento viscoelástico. Las cadenas cargadas de proteoglicanos mantienen una presión osmótica que retiene el agua. Existen diferentes tipos de cartílago (hialino, elástico, fibrocartílago) con variaciones en la composición y organización de su matriz.
Matriz del Hueso
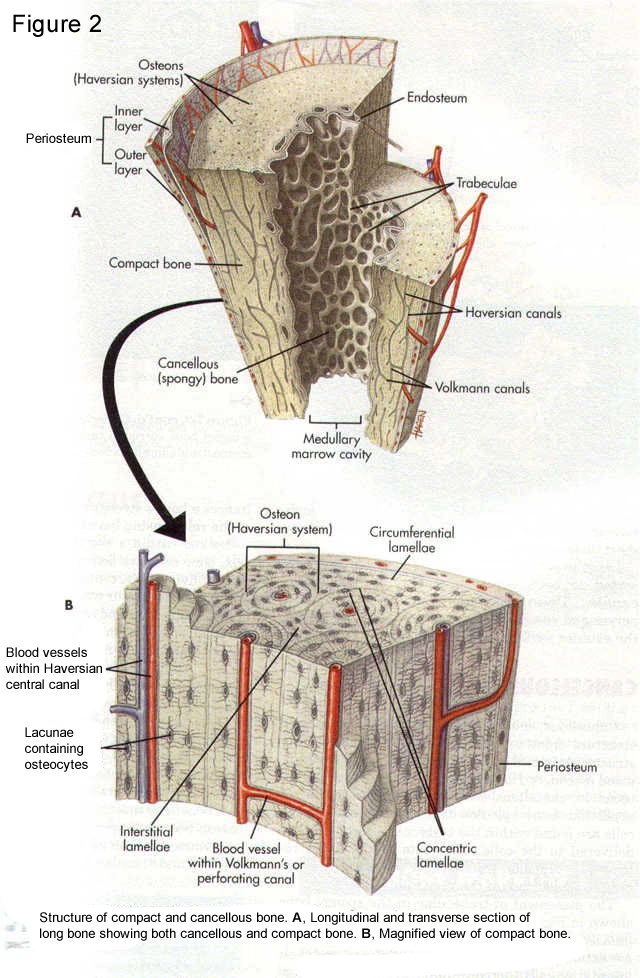
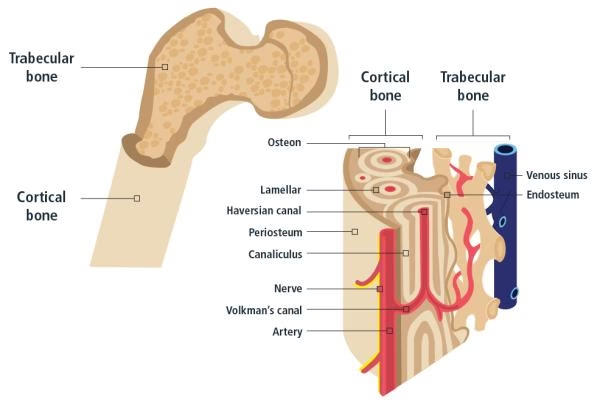
El hueso es un tejido conectivo rígido y fuerte. Su matriz extracelular es única porque está mineralizada. Aunque el texto proporcionado no especifica los minerales exactos, menciona que el hueso es un tejido vivo compuesto por células, proteínas, minerales y vitaminas. La matriz extracelular mineralizada contribuye a sus funciones de soporte, protección de órganos, movimiento y almacenamiento de minerales. Los osteoblastos son las células responsables de producir y secretar la matriz ósea no mineralizada (osteoide), que luego se mineraliza.
Importancia Clínica de la Matriz Extracelular
Dada la importancia fundamental de la matriz extracelular, no es sorprendente que muchas patologías y condiciones médicas estén relacionadas con sus alteraciones. Estas incluyen:
- Enfermedades Autoinmunes del Tejido Conectivo: Un grupo de enfermedades donde el sistema inmunitario ataca los componentes del tejido conectivo. Las cinco reconocidas actualmente son lupus eritematoso sistémico, esclerodermia, miositis, artritis reumatoide y síndrome de Sjogren. También existen la enfermedad indiferenciada del tejido conectivo y los síndromes de solapamiento (como la enfermedad mixta del tejido conectivo).
- Defectos Genéticos: Mutaciones en genes que codifican proteínas de la matriz pueden causar enfermedades graves. Ejemplos incluyen el síndrome de Ehlers-Danlos (defectos en diferentes tipos de colágeno, afectando piel, articulaciones, vasos), el síndrome de Marfan (defecto en fibrilina, afectando tejidos ricos en fibras elásticas como la aorta), la epidermólisis bullosa (fragilidad de la piel) y la osteogénesis imperfecta (mutaciones en colágeno tipo I, huesos frágiles).
- Lesiones y Reparación Tisular: La matriz está directamente involucrada en lesiones como desgarros de tendones, fracturas óseas y lesiones cartilaginosas. La curación de estas lesiones depende de la capacidad de las células para remodelar y resintetizar la matriz.
- Migración Celular y Cáncer: La capacidad de las células cancerosas para degradar la matriz y migrar a través de ella es un paso clave en la metástasis. La regulación de las proteasas de matriz es un área importante de investigación en cáncer.
La matriz extracelular no es solo un andamio; es un entorno dinámico que interactúa constantemente con las células, guiando su comportamiento y respondiendo a las señales del cuerpo. Su estudio es fundamental para comprender la biología tisular y desarrollar tratamientos para una amplia gama de enfermedades.
Tabla Comparativa de Componentes Clave de la Matriz Extracelular
| Componente | Composición Principal | Estructura Típica | Función/Propiedad Principal | Ubicación Clave |
|---|---|---|---|---|
| Colágeno | Proteína fibrosa rica en Pro/Gly | Triple hélice; se ensambla en fibrilas y fibras | Resistencia a la tensión/estiramiento | Tejido conectivo propiamente dicho (tendones, ligamentos, piel), hueso, cartílago, láminas basales |
| Elastina | Proteína hidrofóbica rica en Pro/Gly | Red entrecruzada de fibras | Elasticidad, resiliencia | Piel, vasos sanguíneos, pulmones |
| Glicosaminoglicanos (GAGs) | Polisacáridos no ramificados con carga negativa | Cadenas largas, extendidas | Forman geles hidratados, resisten compresión, difusión | Sustancia fundamental de todos los tejidos conectivos |
| Proteoglicanos | Proteína central + cadenas de GAGs | Moléculas grandes, a menudo forman agregados | Hidratación (sustancia fundamental), regulación de señales, soporte | Sustancia fundamental de tejidos conectivos, superficie celular |
| Fibronectina | Glicoproteína dimérica | Dímero con múltiples dominios | Adhesión celular a la matriz, guía migración | Tejido conectivo, plasma sanguíneo, superficie celular |
| Laminina | Glicoproteína trimérica (α, β, γ) | Forma de cruz asimétrica | Componente estructural clave de láminas basales, adhesión celular | Láminas basales |
| Nidogen (Entactin) | Glicoproteína | Molécula con dominios | Enlaza laminina y colágeno tipo IV | Láminas basales |
Preguntas Frecuentes Sobre la Matriz Extracelular
¿Qué es la matriz extracelular en anatomía?
Es el espacio fuera de las células en los tejidos, llenado por una red organizada de macromoléculas secretadas por las células. Actúa como soporte físico y regula el comportamiento celular.
¿Quién produce la matriz extracelular?
Las células dentro del tejido donde se encuentra. En el tejido conectivo propiamente dicho, son principalmente los fibroblastos. En tejidos especializados, son células como los condroblastos (cartílago) y osteoblastos (hueso).

¿De qué está hecha la matriz extracelular?
Principalmente de polisacáridos (GAGs, a menudo como proteoglicanos) y proteínas fibrosas como colágeno, elastina, fibronectina y laminina, junto con fluido extracelular.
¿Cuál es la función principal de la matriz extracelular?
Proporciona soporte estructural, ayuda a la comunicación y migración celular, resiste fuerzas mecánicas (compresión y tensión), almacena factores de crecimiento y participa en la reparación tisular.
¿De qué está hecha la matriz del cartílago?
Principalmente de colágeno tipo II y proteoglicanos. Es una matriz muy hidratada que le confiere elasticidad y resistencia a la compresión.
¿De qué está hecha la matriz del hueso?
Consiste en componentes extracelulares que están mineralizados. Es una matriz rígida que proporciona soporte y protección.
¿Qué es una lámina basal?
Es una capa delgada y especializada de matriz extracelular que se encuentra debajo de los epitelios, alrededor de células musculares y grasas, y entre ciertas hojas celulares. Está compuesta principalmente por colágeno tipo IV, laminina, nidogen y perlecan.
¿Qué enfermedades están relacionadas con problemas en la matriz extracelular?
Varias, incluyendo enfermedades autoinmunes del tejido conectivo (lupus, esclerodermia) y enfermedades genéticas que afectan proteínas de la matriz (síndrome de Ehlers-Danlos, síndrome de Marfan, osteogénesis imperfecta).
La matriz extracelular es un componente vital y dinámico de nuestra anatomía, fundamental para la integridad y función de nuestros tejidos y órganos. Su compleja composición y las interacciones que mantiene con las células la convierten en un área de estudio apasionante con profundas implicaciones para la salud y la enfermedad.
Si quieres conocer otros artículos parecidos a La Matriz Extracelular: Soporte Vital del Cuerpo puedes visitar la categoría Maquillaje.
