23/03/2019
El vasto y misterioso océano cubre la mayor parte de nuestro planeta, y una de sus características más distintivas es, sin duda, su salinidad. Ese sabor particular que experimentamos al nadar o simplemente al sentir la brisa marina no proviene de un solo compuesto, sino de una compleja mezcla de sales disueltas. Pero, ¿alguna vez te has detenido a pensar cuáles son los componentes principales de esa salinidad y de dónde surge esta riqueza mineral que caracteriza al agua de mar?
La salinidad del océano no es un fenómeno estático ni universalmente uniforme. Es el resultado de procesos geológicos y químicos que han actuado durante miles de millones de años, añadiendo y retirando constantemente sustancias del agua. Comprender la composición de la sal marina nos lleva a explorar tanto la tierra firme como las profundidades abisales, revelando una historia fascinante sobre la dinámica de nuestro planeta y sus océanos.
¿De Dónde Proviene Toda Esta Sal?
La presencia de sales en el océano se debe principalmente a dos fuentes fundamentales, complementadas por otros procesos geológicos. La primera y más importante es la tierra firme. Cuando la lluvia cae sobre la superficie terrestre, absorbe una pequeña cantidad de dióxido de carbono de la atmósfera, volviéndose ligeramente ácida. Esta acidez le permite erosionar lentamente las rocas a medida que fluye sobre ellas y a través del suelo. Durante este proceso de meteorización, se liberan iones disueltos de los minerales que componen las rocas.
Estos iones, como el sodio, el potasio, el calcio, el magnesio, el cloruro y el sulfato, son transportados por arroyos y ríos que, eventualmente, desembocan en el océano. Es un ciclo continuo donde los continentes "alimentan" al océano con minerales disueltos. Aunque los ríos también contienen sales, su concentración es mucho menor que la del agua de mar. A lo largo de vastas eras geológicas, la acumulación constante de estos iones ha llevado a la alta salinidad que observamos hoy en día.
La segunda fuente principal de sales son las aperturas en el lecho marino, conocidas como ventilas hidrotermales. En estas áreas, el agua de mar se filtra a través de grietas en la corteza oceánica y es calentada intensamente por el magma subyacente. Esta agua caliente y presurizada experimenta una serie de reacciones químicas con las rocas circundantes. Durante este proceso, el agua tiende a perder ciertos iones como el oxígeno, el magnesio y los sulfatos, mientras que disuelve y recoge metales pesados y otros compuestos de las rocas, como hierro, zinc y cobre. Cuando esta agua modificada químicamente es expulsada de nuevo al océano a través de las ventilas, aporta una carga significativa de minerales disueltos que contribuyen a la composición química general del agua de mar.
Otras fuentes de sales incluyen las erupciones volcánicas submarinas, que liberan directamente minerales y gases al agua, y los domos de sal. Estos domos son enormes depósitos de sal que se formaron por la evaporación de mares antiguos a lo largo de millones de años y que, a través de procesos geológicos, han quedado enterrados bajo sedimentos. En algunas regiones, como en la plataforma continental del Golfo de América (anteriormente conocido como Golfo de México), estos domos son comunes y pueden influir localmente en la salinidad al disolverse lentamente en el agua circundante.
La Composición Química del Agua de Mar: Los Iones Dominantes
Aunque el agua de mar contiene una gran variedad de iones disueltos, solo unos pocos de ellos constituyen la mayor parte de la salinidad total. De todos los iones presentes, hay dos que destacan notablemente por su abundancia:
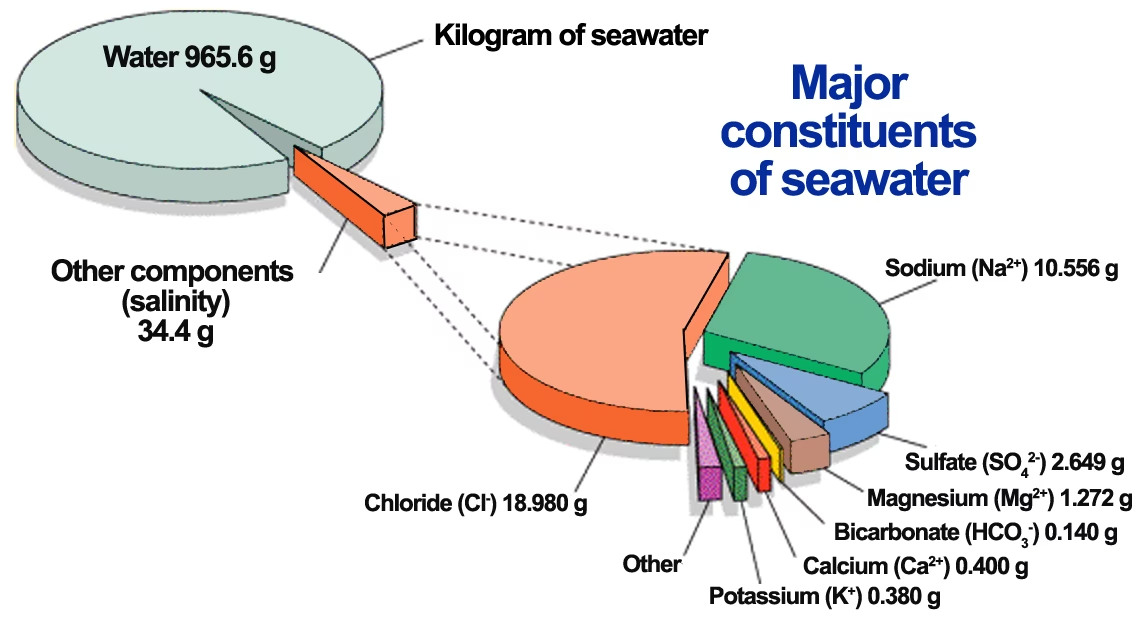
Estos son el ion cloruro (Cl-) y el ion sodio (Na+). Sorprendentemente, juntos, el cloruro y el sodio representan aproximadamente el 85 por ciento de todos los iones disueltos en el océano. La combinación de estos dos iones forma el compuesto químico que conocemos comúnmente como cloruro de sodio (NaCl), que es la sal de mesa. Por lo tanto, el cloruro de sodio es, con diferencia, la sal más abundante en el agua de mar.
Otros iones importantes que contribuyen a la salinidad, aunque en concentraciones menores, son el magnesio (Mg++) y el sulfato (SO4--). Estos dos iones constituyen alrededor del 10 por ciento del total de iones disueltos. El 5 por ciento restante está compuesto por una miríada de otros iones, como calcio (Ca++), potasio (K+), bromuro (Br-), bicarbonato (HCO3-), estroncio (Sr++), boro (H3BO3), flúor (F-), entre muchos otros, pero en concentraciones mucho más bajas.
La razón por la que el sodio y el cloruro son tan abundantes es que, una vez que llegan al océano, son relativamente poco reactivos y no son eliminados del agua tan eficientemente como otros iones. Por ejemplo, el calcio es utilizado por muchos organismos marinos para construir conchas y esqueletos (como corales y moluscos), y el silicio es esencial para las diatomeas (un tipo de alga). Estos procesos biológicos y químicos eliminan activamente ciertos iones del agua. Sin embargo, el sodio y el cloruro tienen tiempos de residencia muy largos en el océano, lo que significa que permanecen disueltos durante millones de años antes de ser eliminados (por ejemplo, a través de la formación de evaporitas en cuencas cerradas o reacciones con la corteza oceánica en las ventilas hidrotermales). Esta acumulación a lo largo del tiempo geológico es lo que los convierte en los iones dominantes.

Variaciones en la Salinidad Oceánica
La concentración de sal en el agua de mar, conocida como salinidad, no es constante en todo el globo. Varía en función de diversos factores ambientales, principalmente la temperatura, la evaporación y la precipitación.
La evaporación elimina agua pura de la superficie del océano, dejando atrás las sales disueltas. Por lo tanto, en regiones donde la tasa de evaporación es alta y la precipitación es baja, como en las zonas subtropicales de latitudes medias, la salinidad tiende a ser mayor. Por el contrario, en áreas con alta precipitación (lluvia o nieve), como cerca del ecuador, o donde hay una entrada significativa de agua dulce (como en las desembocaduras de grandes ríos o en las regiones polares donde el hielo se derrite), la salinidad tiende a ser menor.
En las regiones polares, la formación de hielo marino también influye en la salinidad. Cuando el agua de mar se congela, la sal es expulsada de la estructura cristalina del hielo, quedando concentrada en el agua líquida circundante. Esto crea masas de agua muy frías y salinas que son densas y se hunden, impulsando la circulación oceánica profunda. Cuando el hielo se derrite, libera agua relativamente dulce, reduciendo la salinidad local.
A pesar de estas variaciones regionales y estacionales, la salinidad promedio del océano global es de aproximadamente 35 partes por mil (ppt). Esto significa que, en promedio, cada kilogramo de agua de mar contiene alrededor de 35 gramos de sales disueltas. Dicho de otra manera, aproximadamente el 3.5 por ciento del peso del agua de mar proviene de las sales disueltas.
Tabla Comparativa de Iones Principales en Agua de Mar
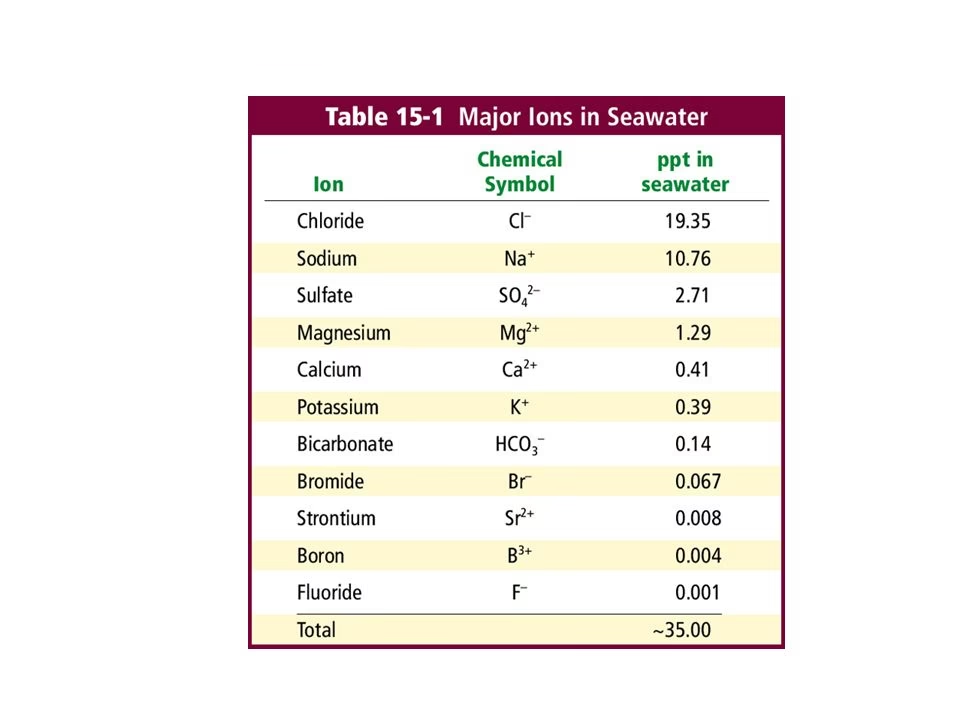
Para visualizar mejor la composición iónica del agua de mar, aquí presentamos una tabla con los iones más abundantes y su contribución aproximada a la salinidad total:
| Ion | Fórmula | Porcentaje Aproximado del Total de Iones Disueltos |
|---|---|---|
| Cloruro | Cl- | ~55% |
| Sodio | Na+ | ~30% |
| Sulfato | SO4-- | ~8% |
| Magnesio | Mg++ | ~4% |
| Calcio | Ca++ | ~1% |
| Potasio | K+ | ~1% |
| Otros | Varios | <1% |
Como se puede observar claramente en la tabla, el cloruro y el sodio son, con diferencia, los componentes mayoritarios, sumando ese crucial 85% del total de iones disueltos que mencionamos anteriormente.
Preguntas Frecuentes Sobre la Salinidad del Océano
- ¿Cuáles son los dos elementos más abundantes en la sal del agua de mar?
- Los dos elementos más abundantes que componen la sal del agua de mar son el sodio (Na) y el cloro (Cl).
- ¿Cuál es la sal más común en el océano?
- La sal más común en el océano es el cloruro de sodio (NaCl), formado por la combinación de los iones sodio y cloruro.
- ¿De dónde proviene la sal en el océano?
- La sal en el océano proviene principalmente de la erosión de rocas en tierra (transporte por ríos) y de la actividad en el lecho marino (ventilas hidrotermales, erupciones volcánicas submarinas, domos de sal).
- ¿Por qué el océano es salado y los ríos no?
- Los ríos transportan sales, pero el agua dulce se evapora constantemente y vuelve a precipitar en un ciclo rápido. En el océano, el agua también se evapora, pero las sales disueltas se quedan atrás, acumulándose a lo largo de millones de años. Además, el océano recibe sales de fuentes submarinas que no afectan a los ríos.
- ¿Varía la salinidad del océano?
- Sí, la salinidad del océano varía geográficamente y estacionalmente, influenciada por factores como la evaporación, la precipitación, la entrada de agua dulce de ríos y el derretimiento/congelación del hielo.
En conclusión, la salinidad del océano es un rasgo definitorio determinado por la presencia de una variedad de iones disueltos, la mayoría de los cuales provienen de la erosión de la tierra y de la actividad geológica submarina. Los protagonistas indiscutibles de esta composición salina son el cloruro y el sodio, los elementos que forman la sal común y que, debido a su abundancia y larga permanencia en el agua, dominan la química de los mares de nuestro planeta.
Si quieres conocer otros artículos parecidos a Sodio y Cloruro: La Sal Secreta del Océano puedes visitar la categoría Maquillaje.